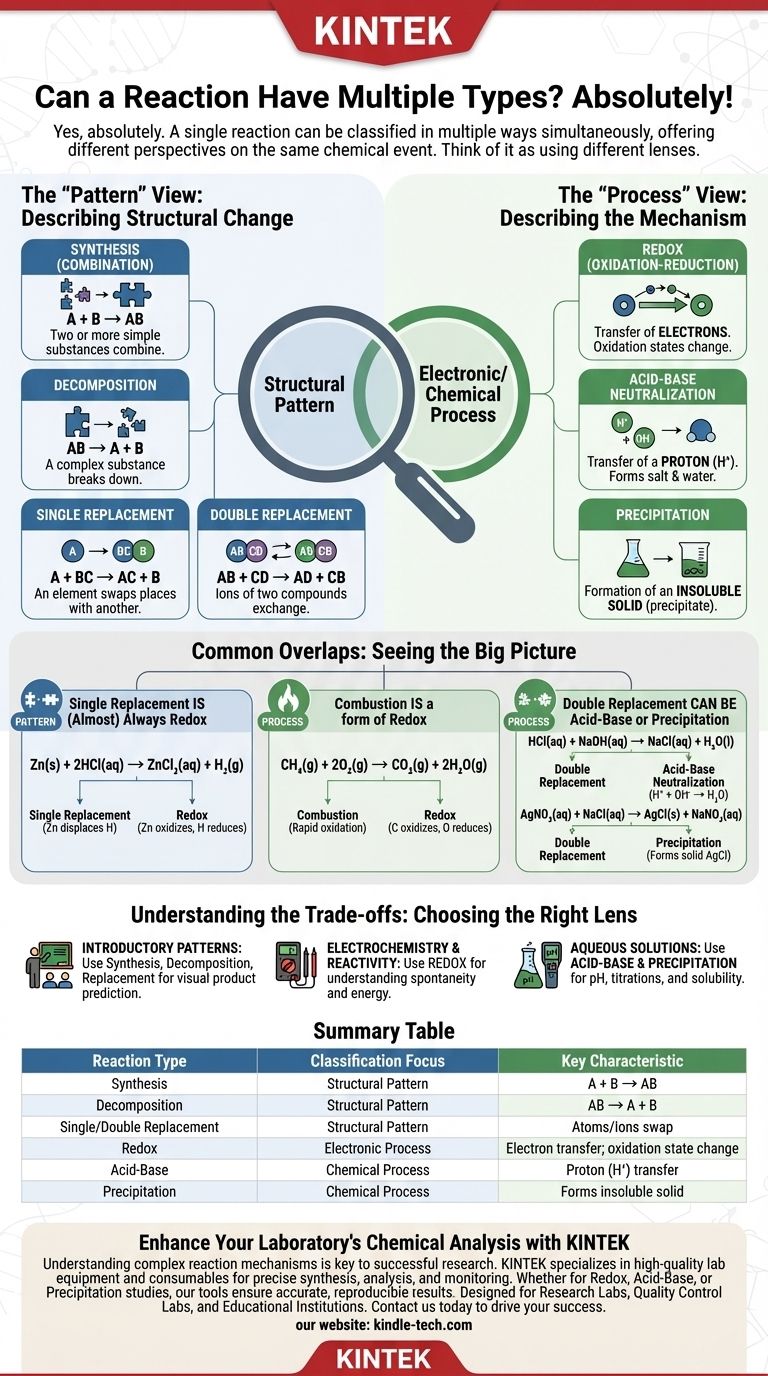
是的,绝对可以。 一个单一的化学反应通常可以同时被归类为多种反应类型。这通常是一个常见的混淆点,因为入门化学通常将反应类型呈现为互斥的类别,但更深入的理解表明它们只是分析同一化学事件的不同视角。
关键在于理解,有些反应类型描述了原子如何重新排列的结构模式(如合成或分解),而另一些则描述了潜在的电子或化学过程(如氧化还原或酸碱反应)。一个单一的反应可以同时展现特定的模式和特定的过程。
为什么简单的标签不够用
我们对反应进行分类的方式取决于我们想要了解它们什么。最初学习的简单类别有助于识别视觉模式,但它们并不总是能解释根本的化学变化。
“模式”视角:描述结构变化
在你的化学教育早期,你学会了通过反应物如何形成产物来识别反应。这些类别描述了转化的整体“形状”。
主要的基于模式的类型有:
- 合成(或化合): 两种或多种简单物质结合形成更复杂的产物(
A + B → AB)。 - 分解: 一种复杂物质分解成更简单的物质(
AB → A + B)。 - 单取代: 一种元素与化合物中的另一种元素交换位置(
A + BC → AC + B)。 - 复分解: 两种化合物的离子交换位置形成两种新化合物(
AB + CD → AD + CB)。
这些标签非常适合根据熟悉的模式快速预测产物。
“过程”视角:描述机制
更复杂的分类描述了转化在分子或电子层面是如何发生的。它们侧重于驱动反应的基本过程。
主要的基于过程的类型包括:
- 氧化还原(氧化-还原): 这种类型涉及电子的转移。反应过程中,一个或多个元素的氧化态发生变化。
- 酸碱中和: 酸和碱反应,通常涉及质子(H⁺ 离子)的转移,形成盐和水。
- 沉淀: 两种水溶液混合,形成不溶性固体(沉淀物)。
这些标签对于理解反应的潜在驱动力至关重要。

你将遇到的常见重叠
了解这些类别如何重叠是巩固理解的最佳方式。你遇到的大多数反应都会有不止一个有效的标签。
单取代(几乎)总是氧化还原反应
考虑锌金属与盐酸的反应:
Zn(s) + 2HCl(aq) → ZnCl₂(aq) + H₂(g)
这是一个经典的单取代反应,因为锌取代了氢。然而,它也是一个氧化还原反应,因为氧化态发生了变化:锌被氧化(0到+2),氢被还原(+1到0)。
燃烧是一种氧化还原反应
甲烷的燃烧是一个很好的例子:
CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g)
虽然我们称之为燃烧,但它本质上也是一个氧化还原反应。碳被氧化(-4到+4),氧被还原(0到-2)。
复分解可以是酸碱反应或沉淀反应
考虑盐酸与氢氧化钠的中和反应:
HCl(aq) + NaOH(aq) → NaCl(aq) + H₂O(l)
这是一个复分解反应;Na⁺ 和 H⁺ 交换了位置。更重要的是,它是酸碱中和的典型例子。
同样,混合硝酸银和氯化钠:
AgNO₃(aq) + NaCl(aq) → AgCl(s) + NaNO₃(aq)
这符合复分解模式,但其最显著的特征是固体的形成,使其成为一个沉淀反应。
理解权衡:分类的目的
选择一个标签不是为了找到唯一的“正确”答案。它是为了为你的特定目标使用最具有描述性和最有用的标签。
简单模式的局限性
将一个反应归类为“单取代”告诉你原子发生了什么,但它没有解释为什么会发生。它没有解释为什么锌与HCl反应而铜不反应。
机制标签的力量
将同一个反应识别为“氧化还原”提供了更深入的见解。它允许你使用活性序列或标准电极电位等概念来预测反应是否会自发发生,并量化所涉及的能量。氧化还原标签解释了“为什么”。
为你的目标做出正确的选择
使用最能服务你目的的分类。目标不是找到一个单一的、排他性的标签,而是应用最相关的标签。
- 如果你的主要重点是在入门课程中识别基本模式: 坚持使用合成、分解以及单/复分解来视觉预测产物。
- 如果你的主要重点是电化学或预测反应性: 氧化还原分类是最重要的视角。
- 如果你的主要重点是处理水溶液、pH值和滴定: 将反应归类为酸碱或沉淀将是最有用的方法。
最终,使用正确的标签取决于你试图回答的关于化学转化的具体问题。
总结表:
| 反应类型 | 分类重点 | 主要特征 |
|---|---|---|
| 合成 | 结构模式 | 两种或多种反应物结合成一种产物(A + B → AB) |
| 分解 | 结构模式 | 一种化合物分解成更简单的物质(AB → A + B) |
| 单取代/复分解 | 结构模式 | 原子或离子在化合物之间交换 |
| 氧化还原 | 电子过程 | 涉及电子转移;氧化态发生变化 |
| 酸碱 | 化学过程 | 涉及质子(H⁺)转移 |
| 沉淀 | 化学过程 | 水溶液中形成不溶性固体 |
使用 KINTEK 提升您的实验室化学分析能力
理解复杂的反应机制是成功研发的关键。在 KINTEK,我们专注于提供高质量的实验室设备和耗材,支持精确的化学合成、分析和过程监控。无论您是在进行氧化还原反应、酸碱滴定还是沉淀研究,我们可靠的工具都能帮助您获得准确和可重复的结果。
我们的产品专为以下用途设计:
- 需要精确温度控制以进行合成和分解反应的研究实验室。
- 需要一致设备进行酸碱和沉淀分析的质量控制实验室。
- 寻求耐用且易于使用的设备以教授基础和高级反应类型的教育机构。
让 KINTEK 成为您提升实验室能力的值得信赖的合作伙伴。立即联系我们,讨论您的具体需求,并了解我们的解决方案如何推动您的成功。
图解指南