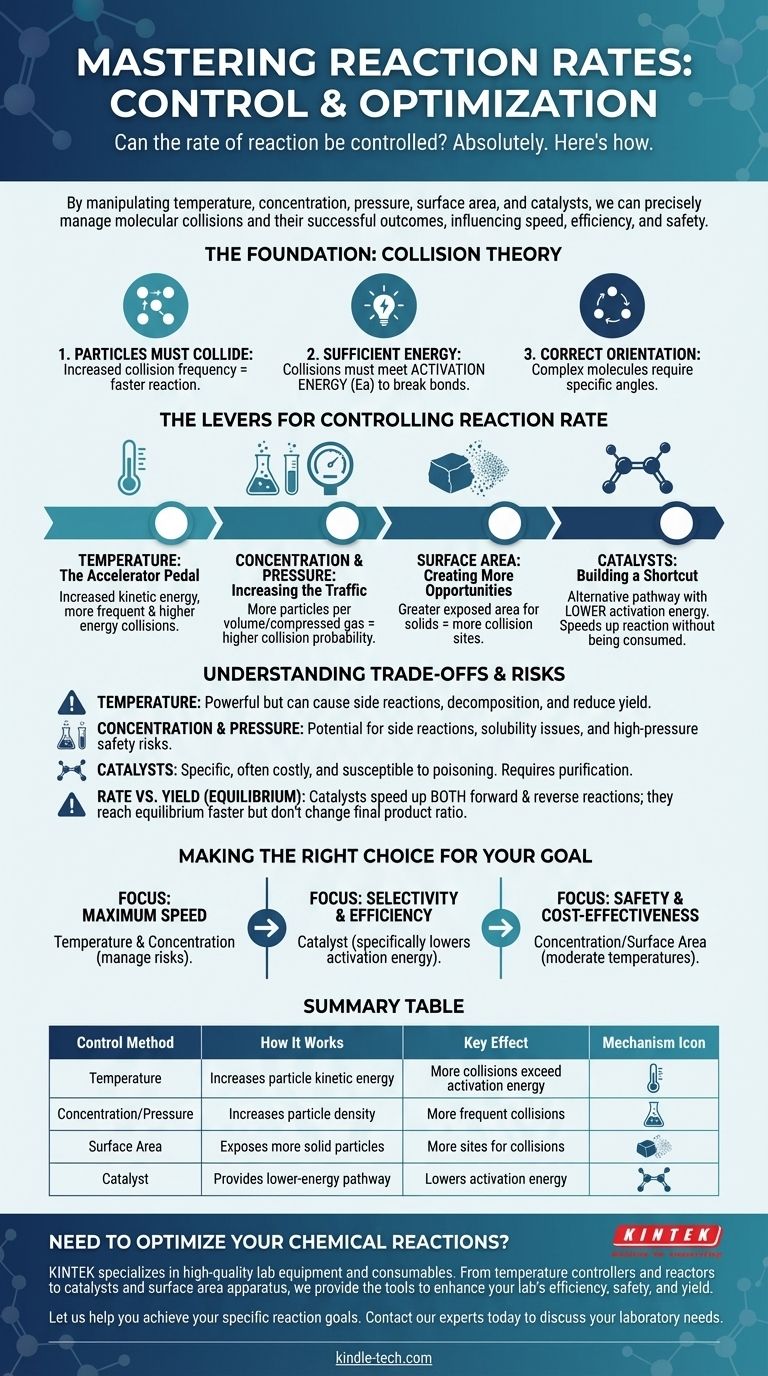
当然可以。化学反应的速率并非固定不变的属性;它可以被精确控制。通过操纵特定的物理和化学因素,我们可以有意识地加速、减缓甚至停止一个反应。主要的控制杠杆是温度、反应物的浓度、压力(对于气体)、表面积(对于固体)以及引入催化剂。
控制反应速率的根本在于管理分子碰撞的频率和能量。每一种方法,从加热物质到添加催化剂,都是通过影响粒子碰撞的频率以及这些碰撞是否成功来发挥作用的。
基础:碰撞理论
要控制一个反应,你必须首先了解它发生的原因。任何反应的速率都受碰撞理论的原理支配,该理论指出,反应发生必须满足三个条件。
1. 粒子必须碰撞
两个或更多分子要发生反应,它们必须首先发生物理接触。粒子碰撞越频繁,它们发生反应的机会就越多,从而提高反应速率。
2. 碰撞必须具有足够的能量
仅仅碰撞是不够的。碰撞的粒子必须拥有最小量的总动能,即活化能(Ea)。这种能量是打破现有化学键以便形成新键所必需的。
能量低于活化能的碰撞将不会成功;粒子只会相互弹开而保持不变。
3. 粒子必须具有正确的取向
对于复杂的分子,碰撞还必须以特定的角度或取向发生。如果在碰撞过程中分子的反应部分没有正确对齐,即使满足能量要求,也不会发生反应。

控制反应速率的杠杆
理解碰撞理论为我们操纵反应速度提供了清晰的路线图。每种控制方法都通过改变成功碰撞所需的一个或多个条件来发挥作用。
温度:加速踏板
提高温度会增加粒子的平均动能。这会产生强大的双重效应。
首先,它使粒子移动得更快,导致更频繁的碰撞。其次,更重要的是,这意味着更大比例的碰撞将具有等于或大于活化能的能量,从而显著提高成功反应的速率。
浓度和压力:增加交通量
增加溶液中反应物的浓度意味着在相同的体积内有更多的粒子。这直接增加了碰撞的概率,从而提高了反应速率。
对于气体,增加压力具有相同的效果。它迫使气体分子更靠近,有效增加了它们的浓度并导致更频繁的碰撞。
表面积:创造更多机会
当固体与液体或气体反应时,这个因素至关重要。通过将固体分解成更小的碎片(例如,从固体块到粉末),你可以显著增加其总表面积。
这使得更多的固体粒子暴露给其他反应物,创造了更多的碰撞位点,从而提高了整体反应速率。
催化剂:建造捷径
催化剂是一种在反应过程中不被消耗但能提高反应速率的物质。它通过提供一个具有较低活化能的替代反应途径来发挥作用。
催化剂不会使粒子更频繁地碰撞或以更高的能量碰撞。相反,它降低了碰撞必须克服的能量“障碍”才能成功,使得反应更容易进行。
理解权衡和风险
虽然这些杠杆是有效的,但它们并非没有后果。选择正确的方法需要理解它们的局限性和潜在的缺点。
温度的粗暴力量
热量是一种强大但无差别的工具。虽然它会加速你想要的反应,但它也会加速任何潜在的副反应。在非常高的温度下,它甚至可能导致反应物或产物分解,降低你的总产率。
浓度和压力的危险
高浓度有时会导致不必要的副反应或溶解度问题。更关键的是,在非常高的压力下操作需要专业的、昂贵的和坚固的设备来管理潜在的容器故障带来的重大安全风险。
催化剂的特异性和成本
催化剂通常具有高度特异性,并且可能非常昂贵(例如,使用铂或钯的催化剂)。它们也可能因杂质而失效,这个过程被称为催化剂中毒,这需要对反应物进行仔细纯化。
速率与产率(平衡)
区分反应速率和反应产率至关重要。对于可逆反应,即可以正向和逆向进行的反应,催化剂会同样加速两个方向的反应。这意味着你将更快地达到平衡,但它不会改变产物与反应物的最终比例。
为你的目标做出正确选择
控制反应的最佳策略完全取决于你的具体目标,无论是速度、效率还是安全。
- 如果你的主要关注点是最大速度:提高温度和浓度是你最直接的工具,但你必须积极管理副反应和安全隐患的风险。
- 如果你的主要关注点是选择性和效率:催化剂通常是最佳选择,因为它可以特异性地降低你所需反应的活化能,而不会促进其他反应。
- 如果你的主要关注点是安全和成本效益:在中等温度下操纵浓度或表面积通常是最易行且风险最低的方法。
掌握这些因素可以让你将化学反应从固定的事件转变为可以精确指导以实现特定结果的动态过程。
总结表:
| 控制方法 | 工作原理 | 关键影响 |
|---|---|---|
| 温度 | 增加粒子动能 | 更多碰撞超过活化能 |
| 浓度/压力 | 增加粒子密度 | 更频繁的碰撞 |
| 表面积 | 暴露更多固体反应物粒子 | 更多碰撞位点 |
| 催化剂 | 提供较低能量的反应途径 | 降低活化能 |
需要优化您的化学反应吗?
精确控制反应速率是成功实验室工作的关键。无论您需要加速合成、提高选择性还是确保安全操作,合适的设备都至关重要。
KINTEK 专注于提供高质量的实验室设备和耗材,帮助您掌握这些变量。从用于管理热量和压力的精密温度控制器和反应器,到专为优化表面积相互作用而设计的各种催化剂和仪器,我们拥有增强您实验室效率、安全性和产率的工具。
让我们帮助您实现特定的反应目标。 立即联系我们的专家,讨论您的实验室需求并找到完美的解决方案。
图解指南