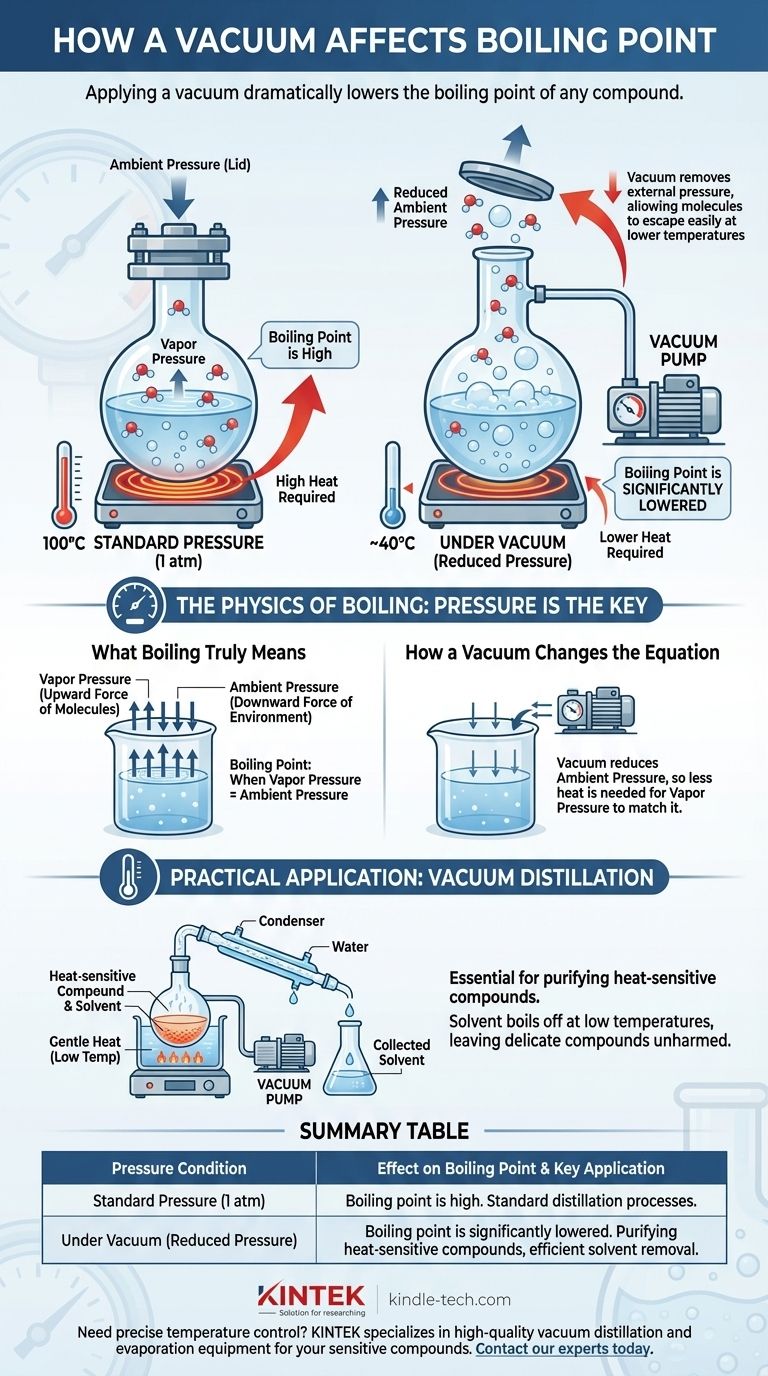
简而言之,施加真空会显著降低任何化合物的沸点。 沸腾并非一个固定的温度,而是液体内部的蒸气压与作用在其表面的外部压力相等的点。通过产生真空,您消除了外部压力,使得分子更容易在远低于常温的温度下从液相中逸出并转化为气体。
液体的沸点不是一个常数;它是周围压力的直接函数。用真空降低此压力,减少了分子转变为气体所需的能量,从而使物质在显著降低的温度下沸腾。
沸腾的物理学:压力是关键
要理解为什么真空具有如此强大的影响,我们必须首先重新定义“沸腾”的实际含义。它更多地与压力之争有关,而非特定的温度。
沸腾的真正含义
沸腾是液体的蒸气压与其环境的环境压力相等的特定物理状态。
在这个平衡点,气泡可以在液体主体内形成并上升到表面。这与仅发生在液体表面的简单蒸发有着本质区别。
蒸气压的作用
每种液体都会产生一定的蒸气压,这是其分子试图逃逸到气相中的固有驱动力。
当您加热液体时,其分子会获得动能。这种增加的能量会使它们更强烈地对抗周围环境,因此,蒸气压随温度升高而增加。
环境压力如何充当“盖子”
我们周围的大气对所有事物,包括液体的表面,施加恒定的压力。您可以将这种环境压力视为一个物理“盖子”,将液体的分子固定在原位。
要使液体沸腾,其蒸气压必须足够强,才能“掀开盖子”。在海平面(1个大气压)下,水必须达到 100°C (212°F) 才能产生足够的蒸气压来实现这一点。

真空如何改变等式
真空泵通过从密闭系统中去除气体分子来工作,从而大幅降低环境压力。这从根本上改变了沸腾所需的条件。
移开“盖子”
施加真空相当于移开那个压力“盖子”。由于推到液体表面的气体分子减少,分子可以更容易地逸出。
这与高海拔地区水沸点较低的原因相同。山上的大气压力较低,因此水要达到其蒸气压与之匹配所需的热量就更少。
新的、更低的沸点
由于外部压力现在低得多,液体不需要像以前那样多的热能就能使自身的蒸气压达到沸点。
结果是,物质将在远低于其标准沸点的温度下沸腾。例如,在足够强的真空下,水可以在室温下沸腾。
实际应用:真空蒸馏
这一原理在化学中对于纯化对热敏感的化合物至关重要。化学家可以将混合物置于真空下并温和加热。
易挥发的溶剂会在非常低的温度下蒸发掉,留下所需的、更精密的化合物,而该化合物从未暴露于可能具有破坏性的高温之下。
理解权衡和陷阱
尽管利用真空降低沸点功能强大,但并非没有挑战,需要仔细考虑。
“爆沸”的风险
在真空下,液体可能会发生剧烈沸腾,这种现象称为爆沸 (bumping)。不均匀的加热可能导致部分液体过热,突然剧烈地汽化。这通常通过使用沸石或持续搅拌来控制。
低挥发性物质的困难
对于分子间作用力非常弱、因此蒸气压非常低的物质(如油或离子液体),即使是高真空也可能无法将沸点降低到足以防止热分解的程度。该技术的作用存在实际限制。
设备和密封完整性
实现和维持深真空需要专业的泵和完全密封的玻璃器皿或容器。即使是微小的泄漏也会影响系统的压力,导致沸点意外升高。
为您的目标做出正确的选择
操纵压力是一种工具,其应用完全取决于您的目标。
- 如果您的主要重点是纯化对热敏感的化合物: 使用真空蒸馏在不会引起分解或不需要的副反应的温度下分离组分。
- 如果您的主要重点是高效去除溶剂: 施加真空,通常伴随旋转(如在旋转蒸发器中),以便在不需要高温的情况下快速蒸发溶剂。
- 如果您的主要重点是对精细材料进行脱水: 使用深真空来降低水的沸点/升华点,从而在低温下(冷冻干燥)脱水,以保持材料的结构。
最终,理解压力和温度之间的关系能让您精确控制物质的物理状态。
总结表:
| 压力条件 | 对沸点的影响 | 关键应用 |
|---|---|---|
| 标准压力 (1 atm) | 沸点处于其标准、较高的温度。 | 标准蒸馏过程。 |
| 真空下 (压力降低) | 沸点显著降低。 | 纯化对热敏感的化合物,高效溶剂去除。 |
需要为您的敏感化合物进行精确的温度控制吗? KINTEK 专注于高质量的真空蒸馏和蒸发设备,包括旋转蒸发器,旨在通过降低沸点来保护您的精细材料。我们的实验室设备确保为研究人员和实验室专业人员提供高效、安全的处理过程。立即联系我们的专家,找到适合您应用的完美真空解决方案!
图解指南