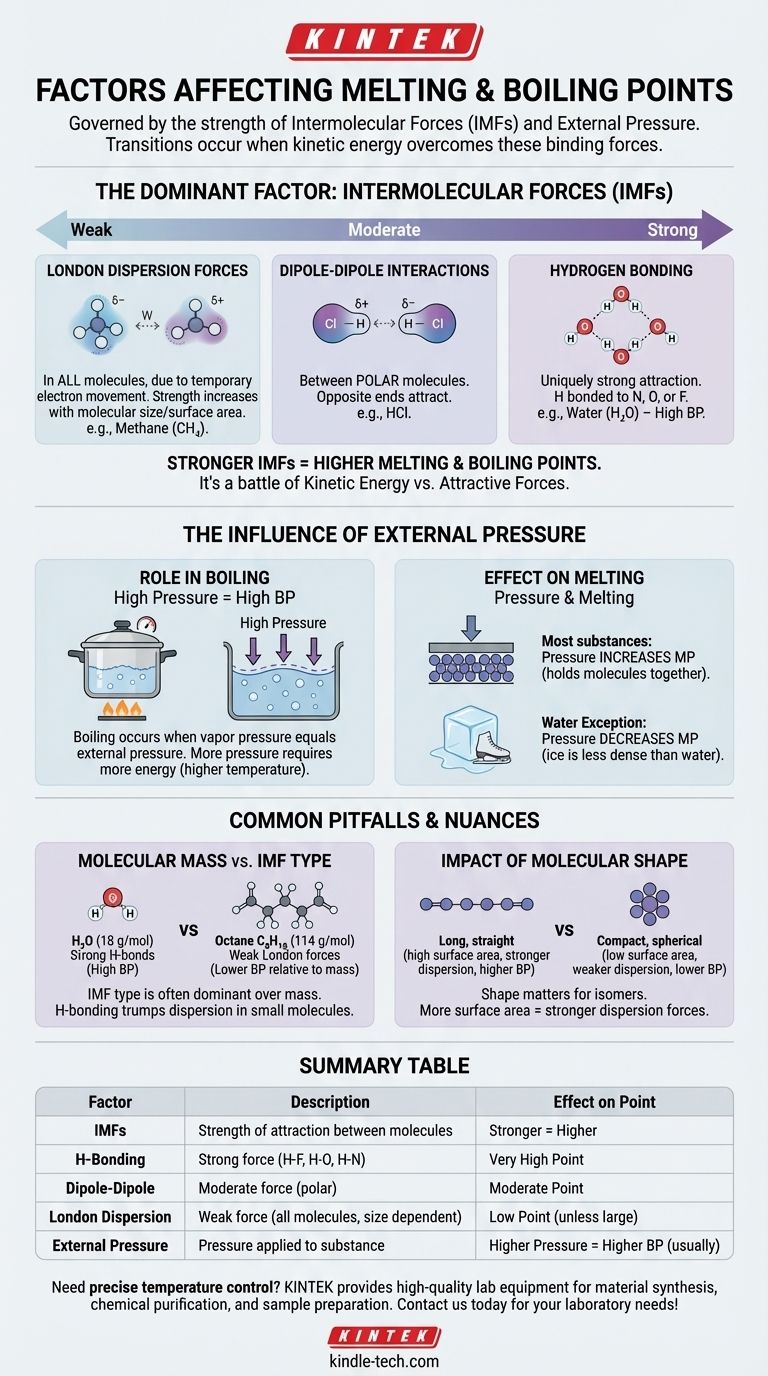
从根本上说,物质的熔点和沸点受两个主要因素支配:维系其分子在一起的分子间作用力 (IMF) 的强度,以及施加在其上的外部压力。本质上,这些转变发生在分子获得足够的能量以克服束缚它们的力和容纳它们的压力时。
核心要点是,熔化和沸腾不仅仅关乎温度;它们是分子动能与将其束缚在其邻居身上的吸引力之间的一场物理较量。这些吸引力越强,将其分离所需的能量就越多。
主导因素:分子间作用力 (IMFs)
决定物质熔点和沸点的最重要因素是其单个分子之间吸引力的强度。这些不是分子内部的强共价键,而是使分子相互粘附的较弱力。
什么是分子间作用力?
将分子间作用力想象成分子层面的磁铁。有些分子就像强大的电磁铁,而另一些则像弱的冰箱磁铁。克服这种“粘性”需要以热量形式存在的能量。
力的等级
分子间作用力的强度各不相同,形成了一个清晰的等级。理解这个等级是预测哪些物质具有更高或更低沸点的关键。
氢键(最强) 这是一种独特的强吸引力,发生在氢与高电负性原子(如氮 (N)、氧 (O) 或氟 (F))键合时。水 (H₂O) 是经典的例子,其强大的氢键是为什么它在体积小的情况下却具有如此高的沸点。
偶极-偶极相互作用(中等) 这些力存在于极性分子之间——分子的一端带有永久性的部分正电荷,另一端带有部分负电荷。这些相反的末端相互吸引,适度地将物质维系在一起。
伦敦色散力(最弱) 这些力存在于所有分子中,由电子的临时、随机运动引起,产生瞬时偶极。虽然它们单独很弱,但随着分子大小和表面积的增加,它们变得更加显著。这就是为什么像辛烷 (C₈H₁₈) 这样较大的分子在室温下是液体,而像甲烷 (CH₄) 这样较小的分子是气体。

外部压力的影响
外部压力就像物质上的物理盖子,使分子更难逸出到下一个相(从固体到液体,或从液体到气体)。
压力在沸腾中的作用
沸腾发生在液体的内部蒸气压等于外部大气压时。
如果你增加外部压力(例如,使用高压锅),你会提高沸点,因为分子需要更多的能量来对抗更强的外部力。
相反,如果你降低外部压力(例如,通过前往高海拔地区),你会降低沸点。这就是为什么水在丹佛的沸点低于海平面。
压力对熔化的影响
对于大多数物质,增加压力会略微提高熔点。这是因为压力有助于将分子保持在固体坚硬、紧密堆积的结构中。
水是一个著名的例外。因为固态冰比液态水密度小,施加压力实际上会使其更容易熔化。这就是为什么滑冰运动员的冰刀可以在冰上滑行。
常见陷阱和细微差别
仅仅看一个因素可能会产生误导。力、质量和形状之间的相互作用产生了重要的细微差别。
分子质量与分子间作用力
虽然沸点通常随摩尔质量的增加而增加,但分子间作用力的类型更为主要。
一个具有强氢键的小分子,如水(18 克/摩尔,沸点 100°C),将比一个只有弱色散力的类似大小的分子,如甲烷(16 克/摩尔,沸点 -161.5°C),具有高得多的沸点。
分子形状的影响
对于具有相同化学式(同分异构体)的分子,形状很重要。长而直的分子具有更大的接触表面积,导致更强的伦敦色散力和更高的沸点。
紧凑的球形分子具有较小的表面积,因此吸引力较弱,沸点较低。
做出正确预测
通过结合这些原理,您可以准确评估为什么不同的物质表现出不同的行为。
- 如果您的主要关注点是比较不同的物质:首先,确定每种物质中存在的最强分子间作用力;这几乎总是决定其相对沸点的主要因素。
- 如果您的主要关注点是改变一种物质的条件:分析外部压力的变化将如何影响相变所需的能量,特别是对于沸腾。
- 如果您遇到意外结果:考虑次要因素,如分子形状或物质独特的密度特性,如水所示。
通过理解这些核心原理,您可以从简单地记忆熔点和沸点,转变为真正理解物质的物理行为。
总结表:
| 因素 | 描述 | 对熔点/沸点的影响 |
|---|---|---|
| 分子间作用力 (IMFs) | 分子间吸引力的强度。 | 作用力越强 = 熔沸点越高 |
| 氢键 | H-F、H-O、H-N 键之间的强作用力。 | 熔沸点非常高 |
| 偶极-偶极 | 极性分子之间的中等作用力。 | 熔沸点中等 |
| 伦敦色散力 | 所有分子中都存在的弱作用力,随尺寸增加而增强。 | 熔沸点低(除非分子很大) |
| 外部压力 | 施加在物质上的压力。 | 压力越高 = 沸点越高(通常) |
您的实验室过程需要精确的温度控制吗?了解相变对于材料合成、化学纯化和样品制备等应用至关重要。在 KINTEK,我们专注于高品质实验室设备,包括烘箱、马弗炉和温度控制系统,旨在提供您的研究所需的准确性和可靠性。让我们的专家帮助您选择适合您特定应用的完美设备。 立即联系我们 讨论您的实验室需求!
图解指南