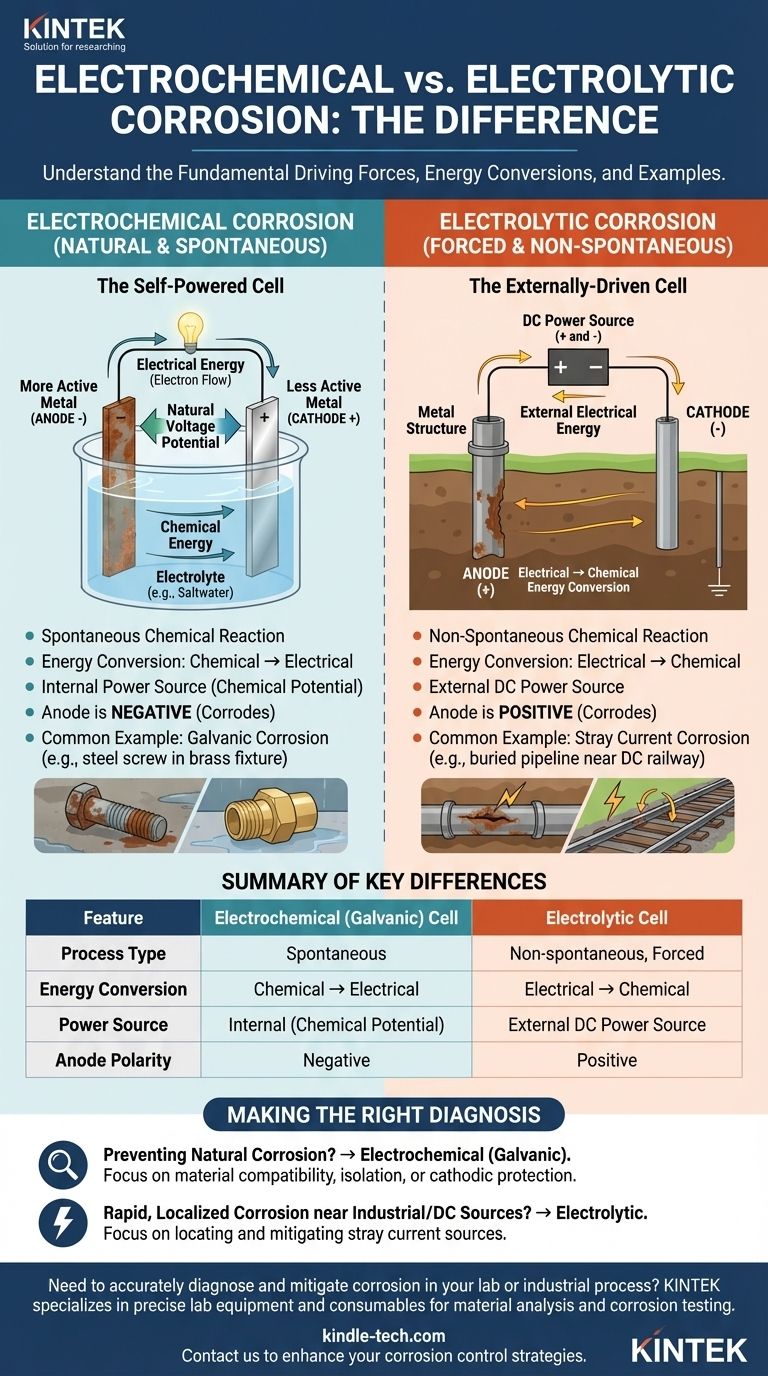
从根本上讲,电解腐蚀电池和电化学腐蚀电池之间的区别在于它们的能量转换和驱动力。电化学电池是一个自发过程,将储存的化学能转化为电能,导致自然腐蚀。相反,电解电池是一个非自发过程,它利用外部电能强制发生化学反应,导致诱导腐蚀。
核心区别在于自发性。电化学腐蚀是自然发生的,就像电池放电一样。电解腐蚀是由外部电源强加于材料的,例如来自铁路系统的杂散直流电流。
电化学电池:腐蚀的自然状态
电化学电池,通常称为原电池,是大多数常见腐蚀形式背后的机制。它是一个自给自足、自然发生的过程。
自发化学反应
当两种不同的金属在电解质(如盐水)存在下发生电接触时,就会形成这种类型的电池。它们之间存在天然的电压电位。
化学活性更强的金属成为阳极(负电极)并发生腐蚀,释放电子。活性较低的金属成为阴极(正电极)并接受这些电子。
能量转换:化学能转化为电能
驱动力是活性更强的金属中储存的化学能的释放。这种化学能以电子从阳极流向阴极的形式直接转化为电能。此过程不需要外部电源。
一个经典的例子是电偶腐蚀,其中钢螺钉(阳极)在潮湿环境中与黄铜固定件(阴极)连接时会迅速生锈。

电解电池:强制腐蚀
电解电池驱动通常不会发生的化学反应。它通过施加外部电源来实现这一点。
非自发化学反应
此过程克服了所涉及材料的自然趋势。外部电源强制金属成为阳极并腐蚀,即使它在其他情况下是稳定的。
当外部提供的直流电 (DC) 离开金属结构进入电解质时,就会发生腐蚀。
能量转换:电能转化为化学能
在这里,来自外部源的电能转化为化学能,表现为腐蚀反应。电池消耗电能来运行。
一个常见的实际场景是杂散电流腐蚀。埋在地下的管道如果靠近直流供电的铁路,可能会吸收泄漏的电流,导致电流流出并进入土壤的管道部分以加速的速度腐蚀。
了解主要区别
虽然这两种过程都涉及阳极、阴极和电解质,但它们的基本特征是相反的。认识到这些差异对于正确诊断和缓解至关重要。
驱动力和电源
最重要的区别是驱动力。电化学电池由材料之间的化学电位差自供电。电解电池由外部直流电源外部供电。
电极的极性
两种电池中阳极和阴极的极性是相反的,这是一个常见的混淆点。
- 在电化学(原)电池中,阳极(发生腐蚀的地方)是负极,阴极是正极。
- 在电解电池中,外部电源使阳极(发生腐蚀的地方)成为正极,阴极是负极。
实际意义
错误识别腐蚀电池类型会导致不正确的解决方案。例如,改变材料配对可以解决电偶腐蚀问题,但对阻止杂散电流腐蚀毫无作用。
做出正确诊断
了解潜在机制是有效控制腐蚀的第一步。您的诊断方法应以可疑电池类型为指导。
- 如果您的主要重点是防止自然腐蚀:您可能正在处理电化学(原)电池。您的解决方案包括选择兼容材料、对它们进行电隔离或应用阴极保护。
- 如果您正在调查工业设备或直流运输附近快速、局部化的腐蚀:您几乎肯定正在处理电解电池。您的首要任务必须是定位并缓解外部杂散电流的来源。
最终,了解腐蚀是自然发生还是受外部影响强制发生,决定了您的整个预防和控制策略。
总结表:
| 特征 | 电化学(原)电池 | 电解电池 |
|---|---|---|
| 过程类型 | 自发 | 非自发,强制 |
| 能量转换 | 化学能 → 电能 | 电能 → 化学能 |
| 电源 | 内部(化学电位) | 外部直流电源 |
| 阳极极性 | 负极 | 正极 |
| 常见示例 | 电偶腐蚀(例如,钢/黄铜) | 杂散电流腐蚀(例如,来自铁路) |
需要在您的实验室或工业过程中准确诊断和缓解腐蚀吗?
了解腐蚀电池的确切类型是有效解决方案的第一步。KINTEK 的专家专门提供材料分析和腐蚀测试所需的精密实验室设备和耗材。无论您是研究电偶反应还是杂散电流效应,我们都拥有支持您研究并确保材料完整性的工具。
立即通过我们的联系表联系我们,讨论您的具体实验室需求,并了解 KINTEK 的解决方案如何增强您的腐蚀控制策略。
图解指南