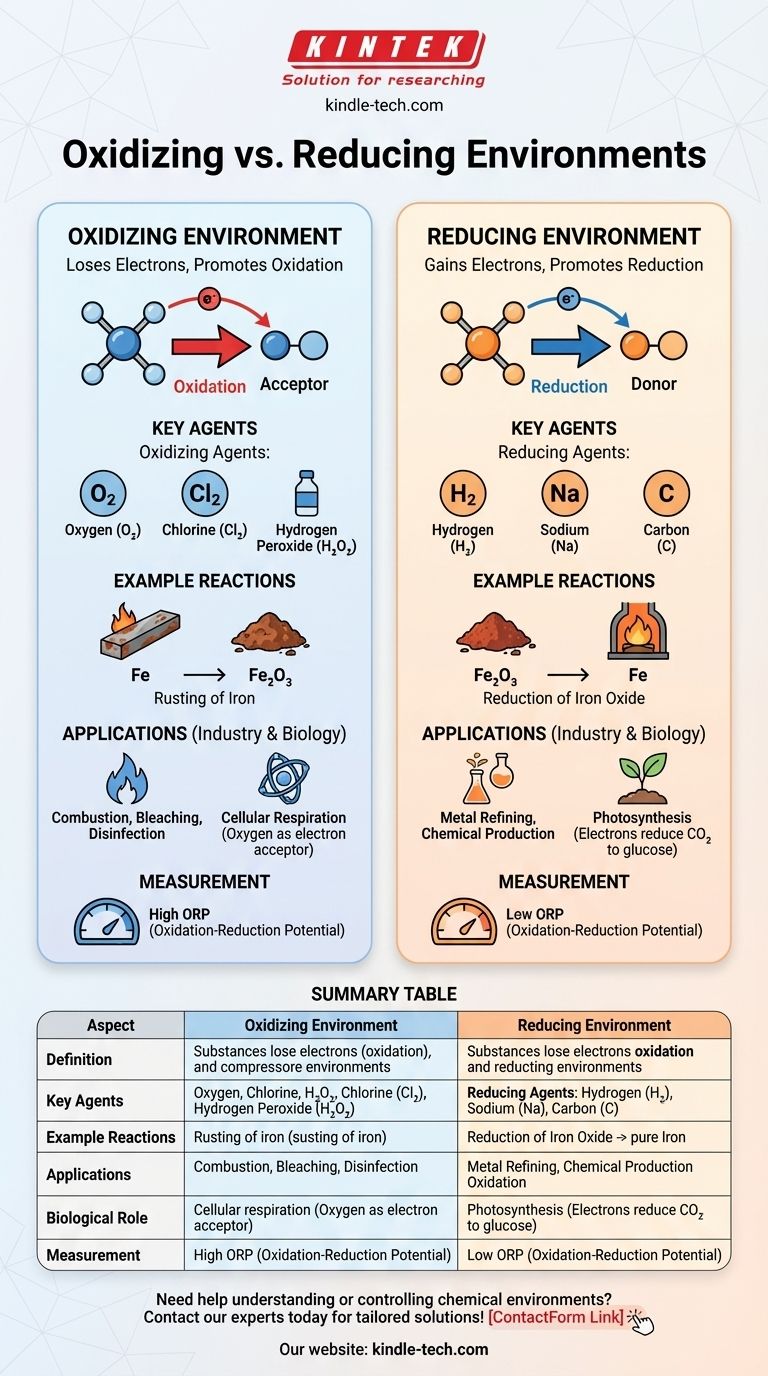
在化学中,氧化环境是指物质倾向于失去电子,促进氧化反应的环境,而还原环境是指物质倾向于获得电子,促进还原反应的环境。主要区别在于电子受体(氧化剂)或电子供体(还原剂)的可用性。氧化环境的特点是存在氧化剂,如氧气或卤素,它们促进电子的失去。相反,还原环境含有还原剂,如氢气或金属,它们促进电子的获得。这些环境在化学反应、工业过程和生物系统中发挥着关键作用。
关键点解释:
-
氧化环境和还原环境的定义:
- 氧化环境:一种化学环境,其中物质更容易失去电子,导致氧化。这种环境富含氧化剂,例如氧气、氯气或其他电子受体。
- 还原环境:一种化学环境,其中物质更容易获得电子,导致还原。这种环境富含还原剂,例如氢气、金属或其他电子供体。
-
氧化剂和还原剂的作用:
- 氧化剂:这些是接受其他物质电子的物质,从而氧化它们。常见例子包括氧气 (O₂)、氯气 (Cl₂) 和过氧化氢 (H₂O₂)。
- 还原剂:这些是向其他物质提供电子的物质,从而还原它们。常见例子包括氢气 (H₂)、钠 (Na) 和碳 (C)。
-
不同环境中的化学反应:
- 氧化环境:在这种环境中,氧化反应占主导地位。例如,铁的生锈发生在氧化环境中,其中铁 (Fe) 失去电子给氧气,形成氧化铁 (Fe₂O₃)。
- 还原环境:在这种环境中,还原反应占主导地位。例如,金属氧化物还原成纯金属发生在还原环境中,例如当碳用于在高炉中将氧化铁还原成铁时。
-
在工业和生物学中的应用:
- 工业应用:氧化环境用于燃烧、漂白和消毒等过程。还原环境在金属精炼和某些化学品的生产等过程中至关重要。
- 生物系统:在生物系统中,氧化环境存在于细胞呼吸等过程中,其中氧气充当最终电子受体。还原环境存在于光合作用等过程中,其中电子被提供以将二氧化碳还原成葡萄糖。
-
测量和控制:
- 氧化还原电位 (ORP):ORP 是衡量化学环境获得或失去电子倾向的指标。高 ORP 表示氧化环境,而低 ORP 表示还原环境。
- 工业过程中的控制:在工业中,控制环境的氧化或还原性质对于优化化学反应、确保产品质量和防止不必要的副反应至关重要。
-
氧化环境和还原环境的例子:
- 氧化环境:地球大气层由于存在氧气而是一个氧化环境。这就是为什么铁等金属暴露在空气中会腐蚀的原因。
- 还原环境:高炉内部是一个还原环境,其中一氧化碳 (CO) 作为还原剂将铁矿石 (Fe₂O₃) 转化为金属铁 (Fe)。
通过了解氧化环境和还原环境之间的差异,化学家和工程师可以更好地控制和优化各种应用中的化学反应,从工业过程到生物系统。

总结表:
| 方面 | 氧化环境 | 还原环境 |
|---|---|---|
| 定义 | 物质因氧气或卤素等电子受体而失去电子(氧化)。 | 物质因氢气或金属等电子供体而获得电子(还原)。 |
| 关键试剂 | 氧化剂:氧气 (O₂)、氯气 (Cl₂)、过氧化氢 (H₂O₂)。 | 还原剂:氢气 (H₂)、钠 (Na)、碳 (C)。 |
| 示例反应 | 铁生锈 (Fe → Fe₂O₃)。 | 氧化铁还原成铁 (Fe₂O₃ → Fe)。 |
| 应用 | 燃烧、漂白、消毒。 | 金属精炼、化学品生产。 |
| 生物作用 | 细胞呼吸(氧气作为电子受体)。 | 光合作用(电子将二氧化碳还原成葡萄糖)。 |
| 测量 | 高氧化还原电位 (ORP)。 | 低氧化还原电位 (ORP)。 |
需要帮助理解或控制化学环境吗?立即联系我们的专家以获取定制解决方案!
图解指南