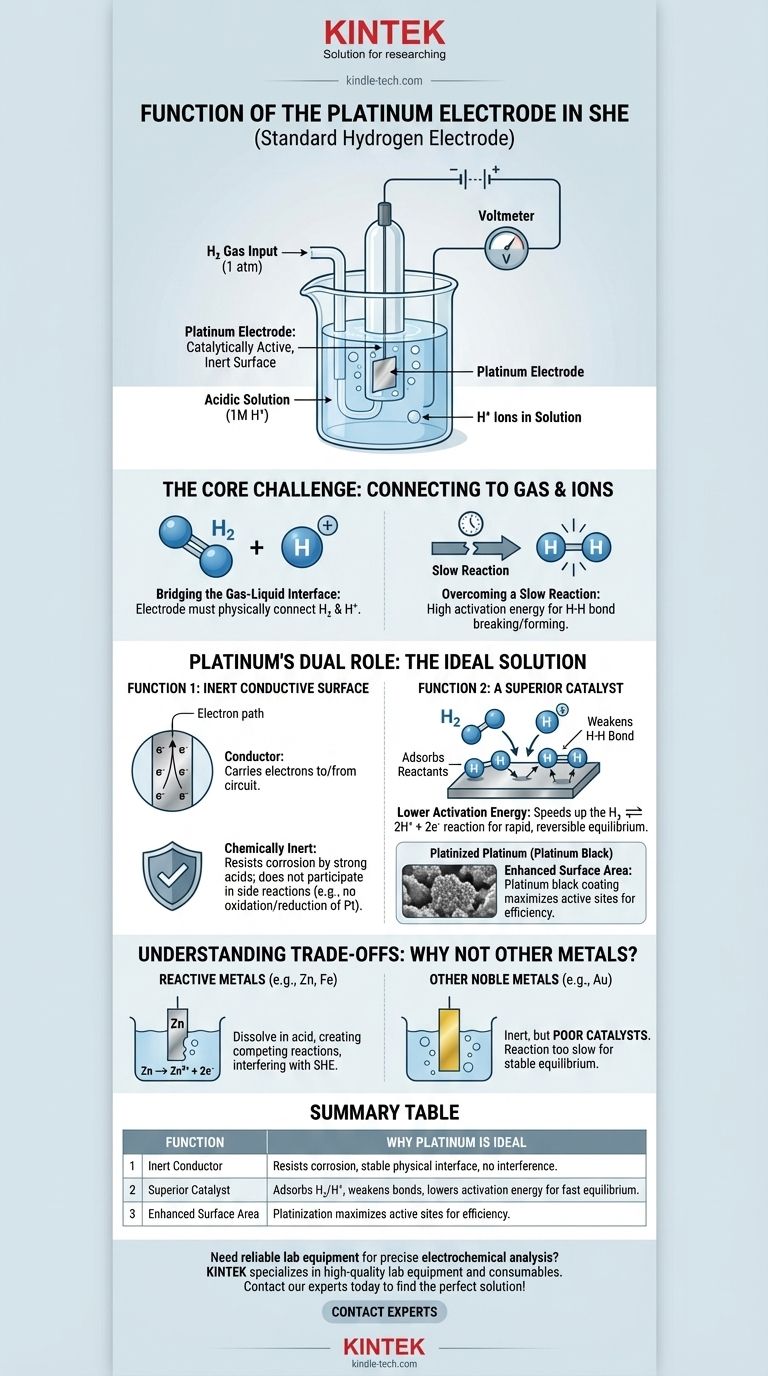
简而言之,标准氢电极(SHE)中的铂电极充当催化活性、惰性的表面。它为氢反应的发生提供了物理位点,并降低了所需的活化能,从而使电池能够达到稳定、可测量的平衡,而电极本身不会被消耗。
SHE 的核心挑战是为涉及气体(H₂)和离子(H⁺)的反应建立可靠的电气连接。铂非常适合此角色,因为它既是氢反应的优良催化剂,又是化学惰性的导体,确保它能促进反应而不对其产生干扰。
核心挑战:将电路连接到气体
要理解铂的功能,我们必须首先认识到构建标准氢电极的基本问题。目标是测量氢氧化还原反应的电势:2H⁺(aq) + 2e⁻ ⇌ H₂(g)。
桥接气液界面
该反应涉及溶解在酸性溶液中的氢离子和鼓泡到电极上的氢气。电极必须存在于这种环境中,以便向外部电路提供或接收电子。
克服缓慢的反应
这种氢反应本身不会快速或有效地发生。分解氢分子中的 H-H 键或结合两个氢离子所需的能量很高。如果没有帮助,系统将无法达到快速且可逆的平衡,使其无法用作标准参考。

铂的双重作用:理想的解决方案
选择铂是因为它能同时解决这两个问题。它既充当惰性物理导体,又充当活性化学催化剂。
功能 1:惰性导电表面
首先,电极必须是导体,以便将电子传导至外部电路或从外部电路接收电子。至关重要的是,它还必须是化学惰性的。
它不能与强酸(通常是 1M HCl)反应,也不能自身被氧化或还原。铂是贵金属,这意味着它具有极强的抗腐蚀和抗溶解能力,使其成为电极的完美稳定物理基础。
功能 2:优异的催化剂
这是铂最关键的功能。它极大地加速了氢氧化还原反应。
铂的表面会吸附氢气分子(H₂)和氢离子(H⁺)。可以将铂表面视为一个工作台,将反应物固定到位,使它们更容易相互作用。
通过吸附氢气,铂表面会削弱强大的共价H-H 键,从而更容易将分子分解成可以被氧化成 H⁺ 离子的单个原子。正是这种催化作用使得反应能够快速且可逆地进行。
“镀铂铂”的作用
为了最大化这种效果,电极通常会涂覆一层细碎的铂粉末,称为铂黑。这种称为镀铂(platinization)的过程,极大地增加了电极的有效表面积,为催化提供了更多的活性位点,确保电极高效运行。
理解权衡:为什么不用其他金属?
研究其他金属为何失效有助于阐明为什么铂是最终的选择。
反应性金属的问题
锌、铁或铝等金属具有很高的反应性。如果将它们置于 SHE 的酸性溶液中,它们会简单地溶解(Zn → Zn²⁺ + 2e⁻)。这会产生一个竞争性的电化学反应,完全干扰氢电极的功能。
其他贵金属的问题
其他惰性金属,如金,可以作为惰性导体。然而,金是氢反应的催化剂方面比铂差得多。虽然金电极不会腐蚀,但反应会太慢而无法建立可靠且可重复的平衡电势,从而失去了“标准”电极的目的。
为您的目标做出正确的选择
理解铂的双重功能是掌握电化学和参考标准的根本原理的关键。
- 如果您的主要重点是反应动力学: 请记住,铂的主要目的是充当非均相催化剂,降低正向和反向氢反应的活化能。
- 如果您的主要重点是电池设计: 请记住,电极材料必须是一种惰性导体,提供稳定的物理界面,而不会参与任何干扰性的副反应。
选择铂是一个深思熟虑的工程选择,它使氢电极能够作为所有电化学测量的通用零点。
摘要表:
| 功能 | 为什么铂是理想选择 |
|---|---|
| 惰性导体 | 在酸中耐腐蚀,提供稳定的物理界面,无干扰反应。 |
| 优异的催化剂 | 吸附 H₂ 和 H⁺,削弱 H-H 键,降低活化能,实现快速、可逆的平衡。 |
| 增强的表面积 | 镀铂(铂黑涂层)最大化活性位点,实现高效性能。 |
需要可靠的实验室设备进行精确的电化学分析吗? KINTEK 专注于高质量的实验室设备和耗材,确保您的实验室获得准确一致的结果。立即联系我们的专家,找到满足您研究需求的完美解决方案!
图解指南
相关产品
- 实验室和工业应用铂片电极
- 旋转铂圆盘电极,用于电化学应用
- 电池实验室应用铂片电极
- 实验室用铂辅助电极
- RRDE 旋转圆盘(圆环圆盘)电极 / 兼容 PINE、日本 ALS、瑞士 Metrohm 玻碳铂













