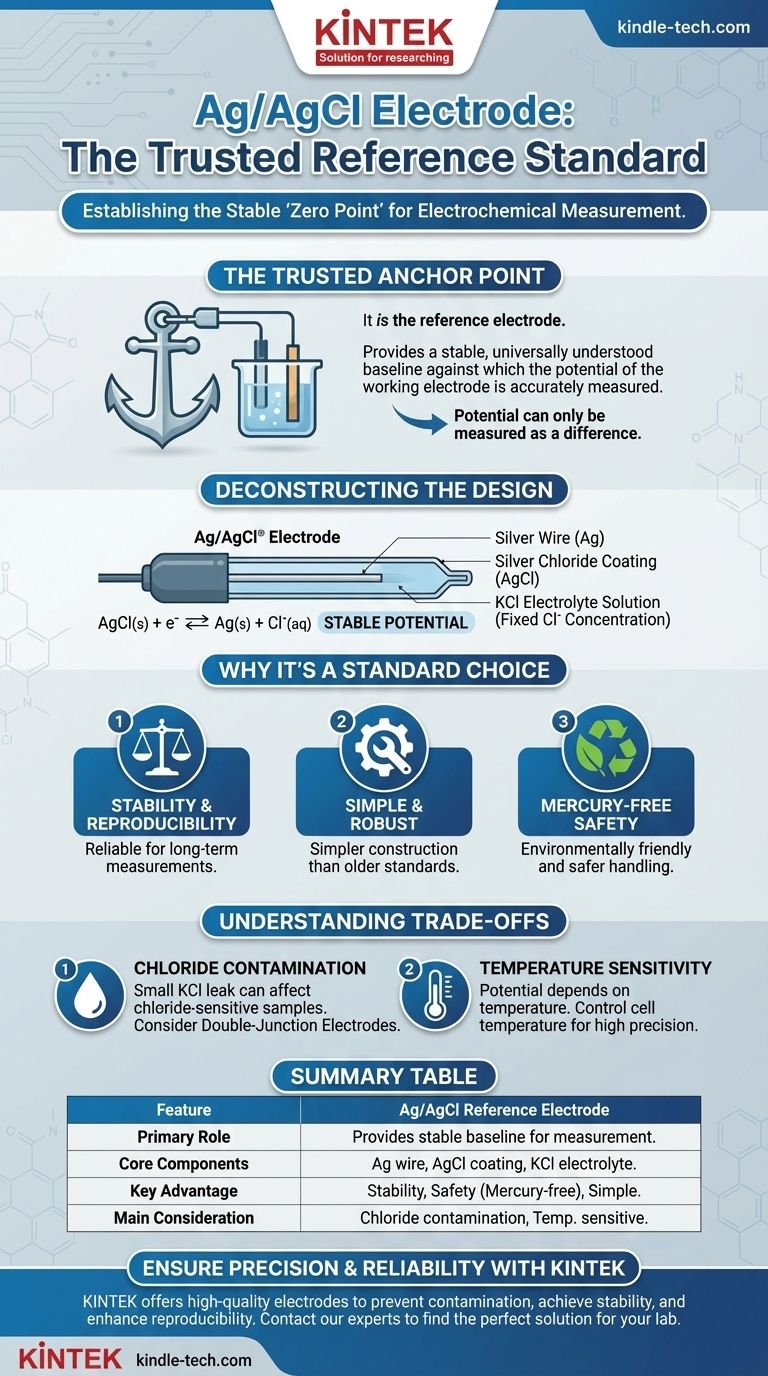
简而言之,银/氯化银 (Ag/AgCl) 电极不是通过参比电极来测量的;它就是参比电极。 它作为一个稳定、国际公认的标准半电池发挥作用。其目的是提供一个恒定且可靠的电位基线,以便准确测量另一个电极(“工作电极”)的电位。
参比电极是电化学中必不可少的工具,因为电位只能测量两点之间的差值。Ag/AgCl 电极为这些测量提供了一个普遍理解、稳定的“零点”,确保结果在不同实验中保持一致和可比较。
是什么让电极成为“参比”?
要理解 Ag/AgCl 电极的作用,首先要弄清楚为什么需要参比。您无法测量单个电极的绝对电位;您只能测量两者之间的电压差。
对稳定基线的需求
在任何电化学测量中,您都对工作电极与样品相互作用时电位的变化感兴趣。为了准确测量这种变化,您需要一个具有恒定、不波动的电位的第二个电极。这个稳定的伙伴就是参比电极。
如何实现稳定性
参比电极的稳定性来自于精心控制的电化学平衡。它是一个半电池反应,其组分是固定的,因此只要温度和组分浓度等条件保持不变,其电位就不会改变。

解析 Ag/AgCl 电极
Ag/AgCl 电极是一种优雅而坚固的设计,通过特定的化学平衡实现高度稳定的电位。
核心组件
电极本身非常简单。它由一根高纯度银丝 (Ag) 组成,该银丝涂有一层氯化银 (AgCl),这是一种微溶于水的盐。
关键电解质
然后将这根涂层银丝浸入固定浓度的氯离子 (Cl⁻) 溶液中。这几乎总是氯化钾 (KCl) 溶液,通常浓度很高(例如,3M 或饱和)。
可逆反应
稳定的电位是由电极表面上的可逆化学反应产生的:
AgCl(s) + e⁻ ⇌ Ag(s) + Cl⁻(aq)
由于银和氯化银是固体,并且填充溶液中氯离子的浓度是固定的,因此该半反应的电位保持不变。
为什么 Ag/AgCl 是标准选择
Ag/AgCl 电极已成为现代实验室中最常见的参比电极,原因有几个实用方面。
稳定性和重现性
该电极在长时间内提供高度稳定和可重现的电位,使其成为常规和研究级测量的可靠标准。
简单、坚固的结构
与饱和甘汞电极 (SCE) 等旧标准相比,Ag/AgCl 电极制造更简单,不易碎,这有助于其广泛采用。
安全和环境影响
至关重要的是,Ag/AgCl 电极是无汞的。这使得它比基于汞的电极更安全,后者由于环境和健康问题在许多实验室中受到限制。
了解权衡
虽然它是行业标准,但没有哪个参比电极是适用于所有情况的完美选择。了解其局限性很重要。
氯化物污染
电极设计有一个多孔玻璃砂芯,可与样品溶液进行电接触。随着时间的推移,少量 KCl 填充溶液可能会泄漏到您的样品中。如果您的样品含有与氯化物反应的物质(例如银离子),这就会成为问题。
温度敏感性
Ag/AgCl 电极的电位取决于温度。对于高精度工作,必须控制并报告电池的温度,或者对数据进行温度校正。
为您的测量做出正确选择
您选择哪种参比电极完全取决于您实验的化学性质和所需的精度水平。
- 如果您的主要重点是常规实验室分析: Ag/AgCl 电极是默认选择,因为它在稳定性、安全性和成本之间取得了出色的平衡。
- 如果您的样品对氯离子敏感: 您必须考虑使用“双液接”Ag/AgCl 电极或替代品,例如汞/硫酸亚汞 (Hg/Hg₂SO₄) 电极,它使用非氯化物填充溶液。
- 如果您需要在各种温度下实现最高精度: 无论您使用哪种参比电极,都必须主动控制电化学电池的温度。
最终,银/氯化银电极是准确和有意义的电化学分析所必需的值得信赖、稳定的锚点。
总结表:
| 特点 | Ag/AgCl 参比电极 |
|---|---|
| 主要作用 | 为测量工作电极提供稳定的电位基线。 |
| 核心组件 | 涂有 AgCl 的银丝,浸泡在 KCl 电解质溶液中。 |
| 主要优点 | 出色的稳定性、安全性(无汞)和简单的结构。 |
| 主要考虑因素 | 潜在的氯化物污染;电位对温度敏感。 |
确保您的电化学测量精确可靠。 正确的参比电极对您实验室的成功至关重要。KINTEK 专注于高质量的实验室设备和耗材,包括一系列针对您特定实验需求量身定制的参比电极。
我们的专家可以帮助您选择理想的电极,以:
- 防止样品污染。
- 实现卓越的测量稳定性。
- 提高结果的重现性。
立即通过我们的安全表格联系我们的团队,讨论您的应用并为您的实验室找到完美的解决方案。
图解指南