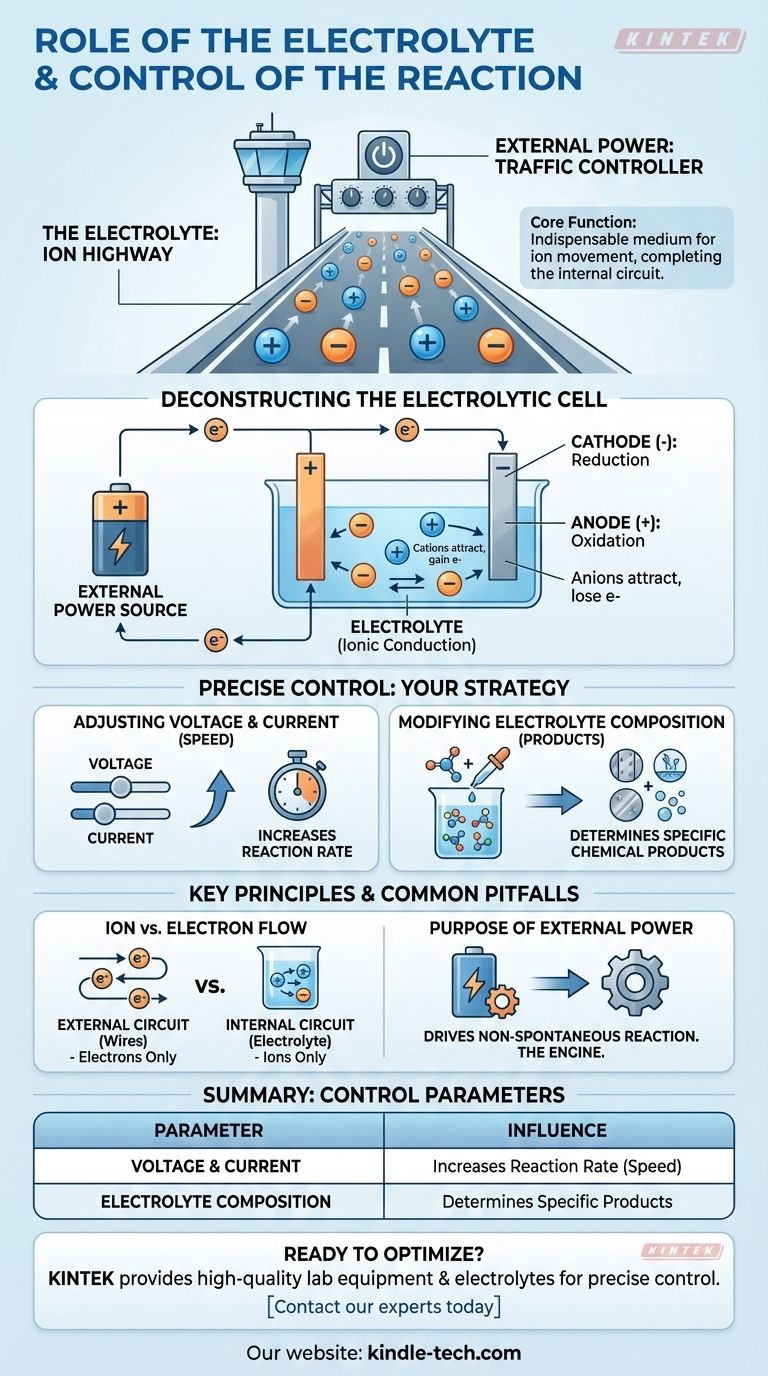
从本质上讲,电解质是细胞内离子移动不可或缺的介质,它完成了化学反应得以发生的电回路。 反应本身是通过操纵外部电输入——特别是电压和电流——以及改变电解质溶液的化学成分来精确控制的。
电解质充当“离子高速公路”,允许带电粒子在电池内部的电极之间传输。外部电源充当“交通管制员”,通过管理电子的流动来决定化学反应的速度和方向。
电解质的基本作用
电化学反应需要一个完整的电路。电解质负责该电路的内部一半,其作用与外部连接的导线有着根本的不同。
什么是电解质?
电解质是一种溶液,通常是水溶液或有机溶液,其中含有解离的离子。
这些自由漂浮的正离子和负离子使得溶液具有导电性。
实现离子传导
电解质的主要功能是离子传导。
虽然电子通过外部导线流动,但离子必须通过溶液在两个电极之间流动。这种带电离子的运动完成了电路,使得反应得以持续。

解析电解池
在电解池中,外部电源驱动一个自身不会发生的化学反应。以下是各个组件如何协同工作。
外部电源
过程始于一个外部电源,如电池或电源。这个电源主动泵送电子,在两个电极之间产生一个电荷差,从而迫使反应进行。
阴极(还原发生的部位)
外部电源将电子推送到阴极,使其带上负电荷。
这种负电荷会吸引电解质中带正电的离子(阳离子)。当这些离子到达阴极时,它们在称为还原的过程中获得电子。
阳极(氧化发生的部位)
同时,外部电源将电子从阳极中抽出,使其带上正电荷。
这种正电荷会吸引电解质中带负电的离子(阴离子)。在阳极,这些离子在称为氧化的过程中失去电子。
反应是如何被精确控制的
通过调整三个关键参数,您可以直接控制电化学反应的结果和速率。
调节电压和电流
电压可以被视为驱动反应的电“压力”,而电流是电子流动的速率。
增加电压和电流通常会提高化学反应发生的速率。这使您能够实时、直接地控制过程速度。
改变电解质成分
发生的具体化学反应取决于电解质中可用的离子。
通过改变电解质的成分——例如,使用不同的盐或溶剂——您可以改变在阳极和阴极上形成的产物。
常见的误区和关键原则
要真正理解该系统,区分电路的两个部分和电池的性质至关重要。
离子运动与电子流动
一个常见的混淆点是电池内部和外部发生的事情之间的区别。
电子只通过外部电路(导线)流动。离子只通过内部电路(电解质)流动。电极表面发生的反应是将这两种不同的路径连接起来的地方。
外部电源的目的
至关重要的是要记住,这个过程描述的是一个电解池。
在这些电池中,电能被用来驱动一个非自发的化学反应。外部电源不是可有可无的;它是使整个过程成为可能的引擎。
根据您的目标做出正确的选择
您的控制策略完全取决于您希望通过反应实现的目标。
- 如果您的主要重点是加快反应速率: 增加施加的电压和电流,以更快地驱动电子和离子的流动。
- 如果您的主要重点是产生特定的化学产物: 小心地选择和控制电解质的成分,以确保所需的离子可用于反应。
- 如果您的主要重点是理解系统的效率: 您必须监测外部电路中的电子流动(电流)和电极上产生的化学变化(离子转化)。
最终,掌握电化学过程意味着理解电解质和外部电路是一个单一、可控系统的两个组成部分。
总结表:
| 控制参数 | 它如何影响反应 |
|---|---|
| 电压和电流 | 增加化学反应的速率(速度)。 |
| 电解质成分 | 决定形成的特定化学产物。 |
准备优化您的电化学过程了吗?
无论您是开发新材料、进行电镀,还是进行精确的分析测试,控制您的电化学反应都至关重要。KINTEK 专注于提供高质量的实验室设备和耗材,以满足您的所有实验室需求,包括可靠的电源和纯电解质。
立即联系我们的专家,讨论我们如何帮助您在实验室中实现精确控制和卓越结果。
图解指南