参考电极简介
定义和功能
参比电极是电化学研究的重要组成部分,它是测量相对于研究电极的电位差的基准。这种测量对于准确评估研究电极在各种条件下的行为至关重要。通常情况下,参比电极的电位是相对于一个 可逆标准氢电极 (RHE) 可逆标准氢电极(RHE)的电位,由于其电位定义明确且稳定,因此被视为通用标准。

参比电极的作用不仅仅是测量,它还能确保电化学数据的一致性和可靠性。通过提供稳定的已知电位,它可以在不同实验和条件下进行精确比较。这种稳定性在腐蚀研究、电池研究和环境监测等领域至关重要,因为在这些领域,即使电位发生微小变化,也会对结果产生重大影响。
在实际应用中,参比电极必须符合特定标准才能确保其有效性。它应表现出 已知且稳定的电位 确保测量结果保持一致。此外,电极必须 可逆 这意味着它可以经历氧化和还原过程而不改变其基本特性。参比电极内的电解质也应具有化学惰性,防止与电解池中的电解质或其他相关物质发生任何不必要的反应。
例如,在典型的设置中,参比电极可能与一个 银/氯化银电极 或 Hg/Hg2SO4 电极 每个电极都有特定的电解质溶液。这些组合可确保参比电极保持稳定和准确,为研究电极的电位测量提供可靠的数据。
良好参比电极的条件
参比电极必须具备几个关键特性,才能在电化学研究中有效发挥作用。首先,它必须保持 已知和稳定的电位 稳定。这种稳定性可确保电位测量的可靠性和一致性,这对准确收集数据至关重要。
其次,电极应 可逆 这意味着它可以进行氧化和还原反应,而电位不会发生显著变化。这种可逆性对于保持电极的完整性和确保电极可反复使用而不会退化至关重要。
此外 电解质 必须仔细选择。它不应与电解池中的电解液或任何相关物质发生化学反应。此类反应可能会改变电极的电位,从而导致错误的测量结果。例如,如果参比电极中的电解质与样品溶液发生反应,可能会导致参比电势发生偏移,从而影响读数的准确性。
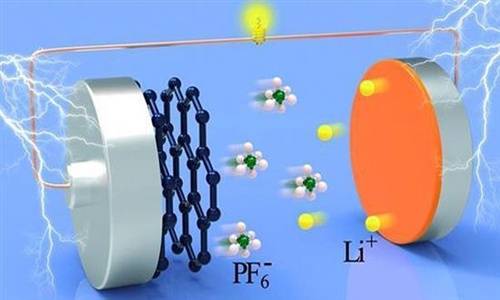
此外,参比电极应 与被测样品兼容 .这种兼容性可确保样品和电解液之间不会产生不必要的化学反应,从而影响电极电位的稳定性。例如,样品中的某些化学物质可能会降低电极材料的性能,这就需要选择合适的材料,如玻璃、环氧树脂或其他合适的物质。
在实际应用中,使用独立的传感(半电池)电极通常更为有效。 半电池)和参比电极会更有效。 如果电极的不同部分预计会有不同的使用寿命,则使用单独的传感电极(半电池)和参比电极通常更为有效。这种分离可以更方便地更换磨损的部件,而无需丢弃整个电极。此外,在某些特殊应用中,使用单独的参比电极不仅实用,而且对于达到所需的精度和效率也是必要的。
例如,在循环伏安法(CV)中,使用一根简单的银丝直接浸入分析溶液作为参比电极理论上是可行的,但并不推荐。Ag+ 离子的缓慢流失可能会与被分析物发生相互作用,而且电解质溶液的任何变化都可能会改变参比电势。最佳做法是使用 Vycor(多孔玻璃)熔块将参比电极与分析溶液隔离。这种设置既能保持电接触,又能最大限度地减少溶液混合,从而保持参比电势的稳定性。
还必须注意防止 vycor 玻璃熔块变干,因为这会导致电解质盐在孔隙中结晶,从而使电极无法使用。定期检查,例如尝试用移液管球将液体挤过熔块,有助于确保其完整性。市售的银/氯化银水溶液参比电极应存放在黑暗处,并浸没在与参比电极内溶液相同的溶液中,通常是饱和氯化钾。随着时间的推移,银/氯化银电极的导线上可能会出现白色堆积物,并偏离其公布的参比电势,因此需要仔细观察并在必要时进行更换。
总之,好的参比电极必须兼具稳定性、可逆性和化学兼容性,才能在电化学实验中提供可靠、准确的电位测量。
参比电极的校准和校正

校准过程
参比电极的校准是一个细致的过程,可确保电化学研究中电位测量的准确性和可靠性。校准过程通常包括建立一个三电极系统,校准中的参比电极作为工作电极。该系统由一个作为参比电极的银/氯化银电极和一个作为对电极的铂(Pt)电极组成。
为实现精确校准,采用了开路电位监测测试法。这种方法包括长期监测工作电极的电位,直到获得稳定的读数。电位曲线的稳定性至关重要,因为它表明参比电极的功能正确且稳定。
| 组件 | 在校准中的作用 |
|---|---|
| 工作电极 | 被测参比电极 |
| 参比电极 | 银/氯化银电极 |
| 对电极 | 铂电极 |
开路电位监测测试方法的优势在于可以识别参比电极电位的任何漂移或不稳定。这种方法是非侵入式的,不需要任何外部电流,是校准期间保持参比电极环境完整性的理想选择。
总之,参比电极的校准过程是确保电化学测量准确性的关键步骤。通过使用三电极系统和开路电位监测测试方法,研究人员可以获得稳定可靠的电位曲线,从而验证参比电极的性能。
校正公式
参比电极的实际电位可通过特定的校正公式准确确定。该公式表示为 ( E_X = x - 0.197 ) ,对于确保电化学测量的精确性和可靠性至关重要。在这个公式中,( x ) 代表参比电极的测量电位,而常数 0.197 则对应于 Ag/AgCl 电极的已知电极电位。
要理解这一校正的意义,必须认识到银/氯化银电极在许多电化学实验中都是标准参比电极。它的电位稳定且有据可查,可以在不同的设置中进行一致的校准。通过从测量值中减去 Ag/AgCl 电极电位,研究人员可以获得参比电极的真实电位,从而消除潜在的差异,提高数据的准确性。
这一校正过程在实验中尤为重要,因为电极电位的微小变化都会对实验结果产生重大影响。因此,公式 ( E_X = x - 0.197 ) 不仅仅是一个数学调整,更是保持电化学测量完整性的关键步骤。
常用参考电极
汞/汞₂SO₄电极
Hg/Hg₂SO₄ 电极由汞和硫酸汞(I)的固体混合物构成,封装在硫酸根离子溶液中。具体来说,电极结构表示为 Hg/Hg₂SO₄(固体)/SO₄²-。 ,通常浸入 0.1M 硫酸盐溶液中。这种设置确保了电极电位的稳定和明确,使其成为各种电化学应用中可靠的参比电极。
与其他参比电极(如银-氯化银电极)不同,汞/汞₂SO₄电极依靠的是 AgCl 在电解液中的沉淀,而汞/汞₂SO₄电极利用的是汞与其硫酸盐化合物之间的固态相互作用。这种独特的结构不仅为电位测量奠定了坚实的基础,还最大限度地降低了污染或不稳定的风险,而这种风险在涉及液-液界面的电极中很常见。
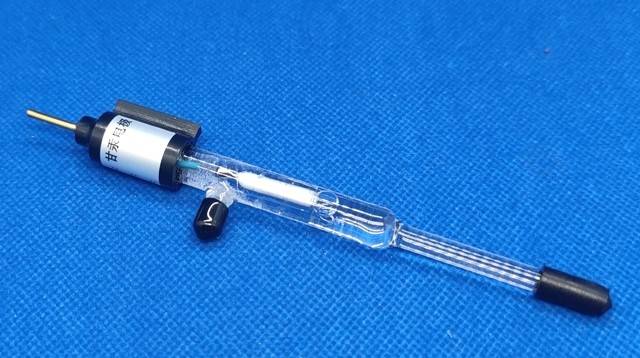
0.1M 硫酸盐溶液可在汞合金周围保持一致的离子环境,从而进一步提高电极的性能。这一浓度是经过精心选择的,目的是在需要足够的离子迁移率与要求电解液干扰最小之间取得平衡。因此,Hg/Hg₂SO₄ 电极在高精度和长期稳定性要求较高的应用中仍然很受欢迎。
饱和汞酸电极
饱和汞酸电极 (SMAE) 是电化学研究中的一个重要组件,其结构由汞(Hg)、氯化亚汞(Hg₂Cl₂,又称甘汞)和饱和氯化钾 (KCl) 溶液组成,因此尤为著名。该电极旨在保持稳定且可重复的电位,这对各种电化学实验中的精确测量至关重要。
SMAE 的结构简单而高效。它的底部是一个水银池,水银池上沉积了一层固体甘汞。该甘汞层是汞和电解质溶液之间的中间层。内置的饱和氯化钾溶液可确保电极保持平衡状态,提供稳定的参考电位。
SMAE 的主要优势之一是能够在饱和 KCl 环境中运行,这有助于保持高浓度的氯离子。这种饱和度至关重要,因为它能最大限度地减少电位波动,确保长时间保持稳定的参考电位,因此特别适合长期实验。
总之,SMAE 的设计采用汞/汞₂氯₂(固体)/氯化钾结构,并使用饱和氯化钾溶液,可提供稳定可靠的参考电位,是许多电化学应用的首选。
银/氯化银电极
银/氯化银(Ag/AgCl)电极是一种广泛使用的参比电极,因为与 Calomel 电极等其他参比电极相比,它成本效益高,毒性低。这种电极由银丝(Ag)和一层固体氯化银(AgCl)组成,然后将银丝浸入氯化钾(KCl)和氯化银(AgCl)的饱和溶液中。电极的结构可表示为 Ag/AgCl(固体)/KCl。
该电极根据以下半反应进行操作:
\text{AgCl(s)} + \text{e}^- \leftrightarrow \text{Ag(s)} + \text{Cl}^-(\text{sat'd}) $$$
在 25°C 时,相对于标准氢电极(SHE),该反应产生的电位为 0.197 V。由于氯化钾和氯化银对氯离子活性的影响并不完全一致,因此该值略微偏离标准电极电位 (E0) 0.222 V。
Ag/AgCl 电极受到青睐有几个原因:
- 稳定性:它能长时间保持稳定的半电池电位。
- 温度相关性:电位变化约为 0.5 - 1.0 mV/°C,相对较小。
- 饱和溶液:电解质的蒸发损失不会改变溶液的饱和性质,从而保持电极的电位。
银/氯化银参比电极的示意图通常以插图的形式显示,使人清楚直观地了解其构造和操作。
汞/氧化汞电极
汞/氧化汞电极(MMO 电极)是电化学研究中的关键部件,具有独特的结构。该电极由金属汞(Hg)层和固体氧化汞(HgO)层直接接触组成,全部浸入浓氢氧化钾(KOH)溶液中。具体来说,内置溶液通常是 1M 的 KOH 溶液,这对保持电极的稳定性和性能起着至关重要的作用。
MMO 电极因其能够提供稳定且可重复的电位而备受推崇,是各种电化学应用的理想选择。KOH 溶液不仅能确保电极的功能,还有助于防止污染和保持电极的使用寿命。这种设置使 MMO 电极能够有效地充当参比电极,提供一致的电位读数,这对精确的电化学测量至关重要。
总之,氧化汞/汞电极因其坚固的结构和 1M KOH 溶液的使用而脱颖而出,这共同造就了它在电化学研究中的可靠性和有效性。
参比电极的选择和维护
选择标准
在选择参比电极时,必须确保内置溶液与研究系统相匹配,以防止任何潜在的污染。这种匹配至关重要,因为参比电极的电解质不应与电解池中的电解质或相关物质发生反应,以免影响测量的准确性。
例如,在使用 H₂SO₄ 溶液时 时 Hg/Hg₂SO₄ 电极是理想的选择。 是理想的选择。这种电极的结构为 Hg/Hg₂SO₄(固态)/SO₄²-,内置 0.1M 硫酸盐溶液,非常适合硫酸环境。另一方面,对于 氯化物溶液 电极 银/氯化银电极 是首选。这种电极的结构为 Ag/AgCl(固体)/KCl,内置 0.1M KCl 溶液,是氯化物研究系统的最佳选择。
| 溶液类型 | 推荐电极 | 电极结构 | 内置溶液 |
|---|---|---|---|
| H₂SO₄ 溶液 | 汞/汞₂SO₄电极 | 汞/汞₂SO₄(固体)/SO₄²- | 0.1M 硫酸盐溶液 |
| 氯化物溶液 | 银/氯化银电极 | 银/氯化银(固体)/氯化钾 | 0.1M KCl 溶液 |
将参比电极与溶液类型仔细匹配,可以大大降低污染风险,确保电化学测量更可靠、更准确。
维护提示
正确维护参比电极对保持其准确性和使用寿命至关重要。为确保最佳性能,请遵循以下基本维护提示:
-
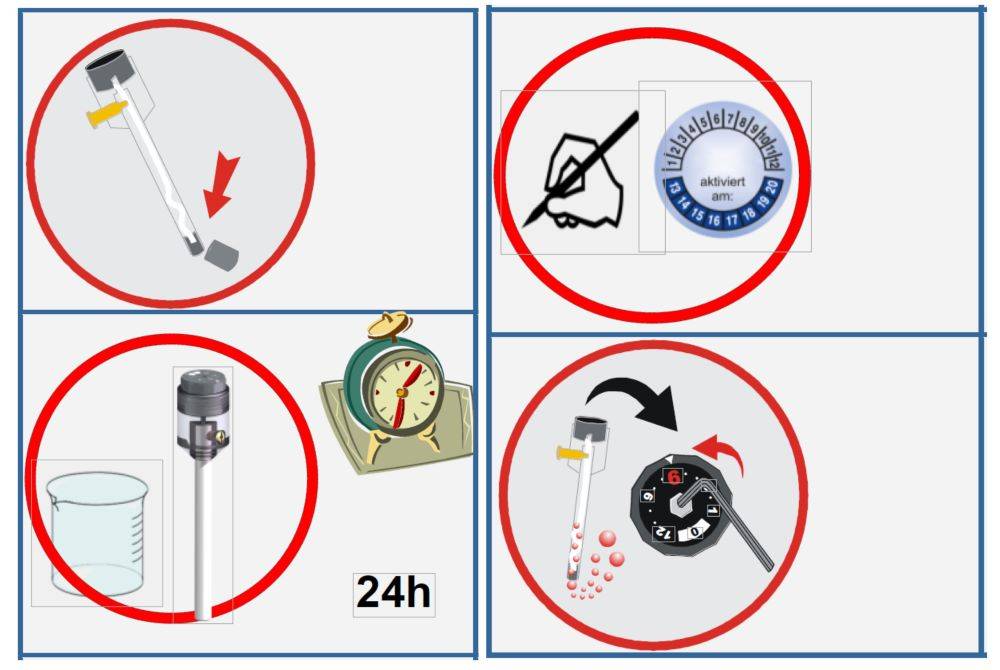
储存条件:将参比电极储存在室温下,以防止极端温度引起的潜在波动。此外,电极应避免光线直射,以防材料降解。
-
填充液管理:定期更换填充液,以保持电极电位的稳定性。更换频率取决于使用率,但通常建议每隔几周检查和更换一次溶液,以确保一致性。
-
气泡预防:确保内置溶液中没有气泡。气泡会产生障碍,破坏电连接,从而影响电极的性能。定期检查溶液,并轻轻敲击电极以清除残留的空气。
通过坚持这些维护方法,您可以显著提高参比电极的可靠性和使用寿命,确保电化学研究结果的准确性和一致性。



















