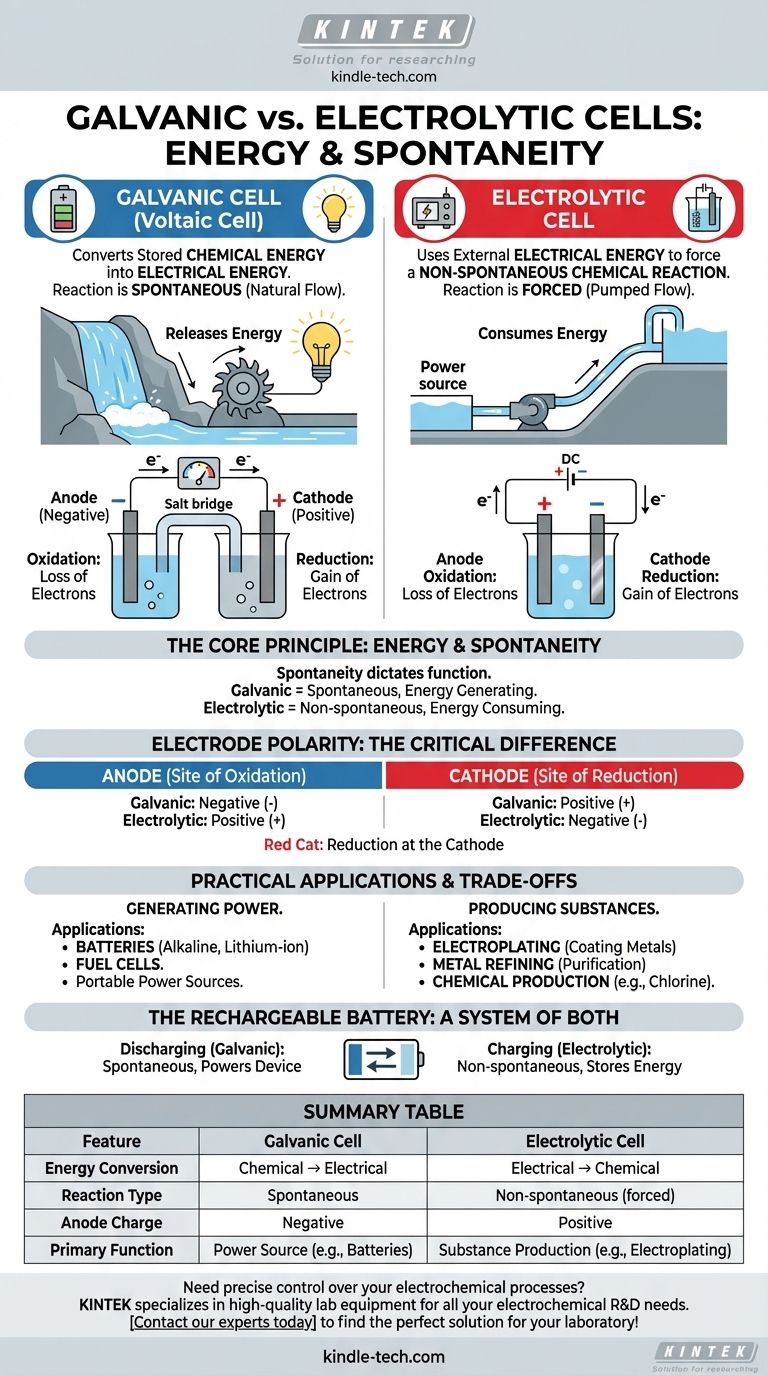
从核心来看,原电池和电解池之间的区别在于能量转换的方向。原电池(或伏打电池)通过自发反应将储存的化学能转化为电能,就像电池为设备供电一样。相反,电解池利用外部电能强制进行非自发化学反应,例如在金属电镀中。
根本区别在于自发性。原电池利用自身会发生的化学反应,释放能量作为电能。电解池则利用电能强制进行否则不会发生的化学反应。
核心原理:能量与自发性
任何电化学电池的行为都取决于其内部氧化还原反应是自发的还是非自发的。这一单一原理决定了其功能和结构。
原电池:产生能量
在原电池中,化学反应是自发的。这意味着反应物比产物具有更高的势能,反应自然进行,释放能量。
这种释放的能量驱动电子通过外部电路,产生电流。把它想象成一个瀑布:水自然向下流动,我们可以在其路径中放置一个涡轮机来发电。
电解池:消耗能量
在电解池中,所需的化学反应是非自发的。产物处于比反应物更高的能量状态,因此反应不会自行发生。
为了使其发生,我们必须从外部电源(如电池或电源)提供能量。这种外部电压强制电子逆着其自然方向移动,驱动反应。这就像使用水泵将水抽到高处一样。

该原理如何定义电池组件
虽然阳极和阴极的基本定义保持不变,但它们的电荷(极性)在两种电池类型之间是相反的。这是一个常见的混淆点,但它是自发性的直接结果。
阳极:始终是氧化发生的地方
在两种电池类型中,阳极都被定义为发生氧化(失去电子)的电极。
阴极:始终是还原发生的地方
同样,在两种电池类型中,阴极都是发生还原(获得电子)的电极。一个简单的助记符是“红猫”(Red Cat,还原在阴极)。
关键区别:电极极性
在原电池中,阳极处自发的氧化释放出电子流。这种负电荷的积累使阳极为负极,而吸引电子的阴极为正极。
在电解池中,使用外部电源。其正极连接到阳极,在那里它强制将电子从化学物质中拉走,导致氧化。因此,阳极为正极,阴极为负极。
实际应用和权衡
产生能量和消耗能量之间的差异导致这两种类型的电池在实际应用中完全不同。
原电池的实践:便携式电源
原电池被设计为电源。它们的主要应用是电池,从一次性碱性电池到手机和汽车中的可充电锂离子电池。
燃料电池是另一种原电池,只要供应燃料(如氢气),就能持续发电。
电解池的实践:制造和精炼
电解池是用于生产材料的工业主力。主要应用包括电镀(在物体上镀一层薄金属)和铜、铝等金属的提纯。
它们对于生产关键工业化学品也至关重要,例如从盐水(盐卤)中生产氯气和氢氧化钠。
可充电电池:两者的系统
可充电电池是这两种原理的完美例证。当它为您的设备供电时,它充当原电池,进行自发反应。当您插入电源充电时,外部电源反转该过程,将其变成电解池,以驱动非自发反应并恢复初始反应物。
为您的目标做出正确选择
您对选择哪种电池的理解完全取决于您是需要产生能量还是产生物质。
- 如果您的主要重点是从化学反应中产生能量:您正在使用原电池,其中自发过程产生电流。
- 如果您的主要重点是利用电能制造物质:您正在使用电解池,其中外部电压驱动非自发化学变化。
- 如果您的主要重点是储存和重复使用电能:您正在处理一个可充电系统,它在电解池(充电)和原电池(放电)之间交替。
归根结底,这两种电池类型是同一电化学硬币的两面,由能量流的方向定义。
总结表:
| 特点 | 原电池 | 电解池 |
|---|---|---|
| 能量转换 | 化学能 → 电能 | 电能 → 化学能 |
| 反应类型 | 自发 | 非自发(强制) |
| 阳极电荷 | 负 | 正 |
| 主要功能 | 电源(例如,电池) | 物质生产(例如,电镀) |
需要精确控制您的电化学过程吗?正确的实验室设备对于准确的结果至关重要,无论您是开发新的电池材料还是改进金属电镀技术。KINTEK 专注于为您的所有电化学研究和开发需求提供高质量的实验室设备和耗材。立即联系我们的专家,为您的实验室找到完美的解决方案!
图解指南