在电化学中,电极最好不要理解为三种不同的类型,而是通过两个主要的分类系统来理解。 最基本的系统根据其功能定义电极:要么是发生氧化反应的阳极,要么是发生还原反应的阴极。第二个同样重要的系统根据其材料组成和在反应中的作用进行分类:要么是活性电极(参与反应),要么是惰性电极(为反应提供表面)。
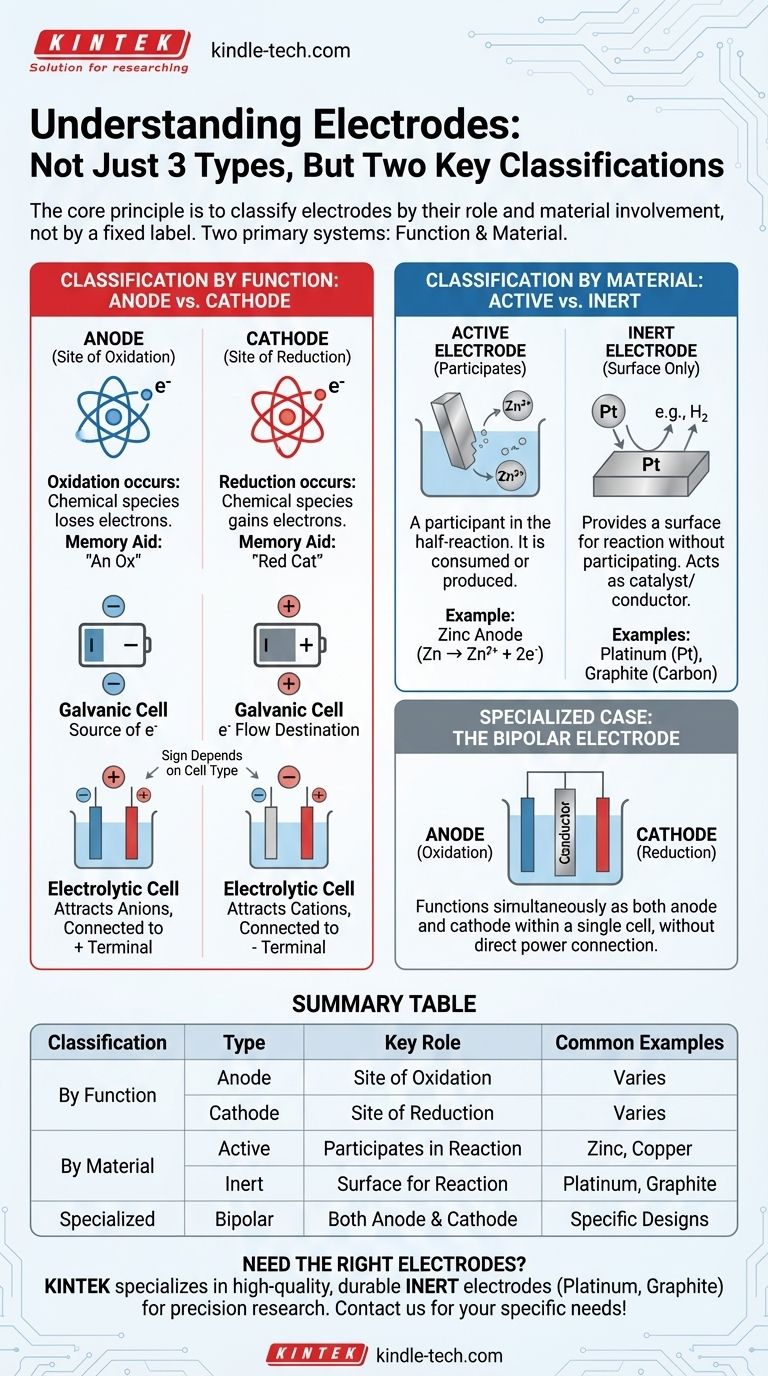
核心原则是根据电极的作用而不是固定标签来对其进行分类。两个最关键的分类是基于功能(阳极与阴极)和材料参与(活性与惰性)。理解这两对是分析任何电化学电池的关键。
按功能分类:阳极与阴极
定义电极最基本的方法是根据其表面发生的化学过程。这个作用会根据电流的流动而改变。
阳极:氧化反应的场所
阳极被定义为发生氧化反应的电极。这是一个化学物质失去电子的过程。
一个简单的记忆辅助是 "An Ox"(阳极是氧化反应 Anode is Oxidation)。
阴极:还原反应的场所
阴极是发生还原反应的电极。这是一个化学物质获得电子的过程。
一个相应的记忆辅助是 "Red Cat"(阴极发生还原反应 Reduction at the Cathode)。

关键区别:正负号与功能
一个常见的困惑是阳极和阴极是正极还是负极。这完全取决于电化学电池的类型。
在原电池中(如电池)
原电池通过自发反应产生电能。
- 阳极是负极 (-)。它是氧化反应中电子的来源。
- 阴极是正极 (+)。它是电子流向以引起还原反应的地方。
在电解池中(如电镀)
电解池利用外部电能驱动非自发反应。
- 阳极是正极 (+)。它连接到电源的正极,吸引阴离子被氧化。
- 阴极是负极 (-)。它连接到电源的负极,吸引阳离子被还原。
按材料分类:活性与惰性
第二个主要分类描述了电极材料本身是否参与化学反应。
活性电极
活性电极(或反应性电极)是半反应的参与者。它由被氧化或作为还原产物的材料制成。
例如,在锌铜电池中,锌阳极会物理溶解(氧化)成锌离子(Zn → Zn²⁺ + 2e⁻)。电极本身被消耗。
惰性电极
惰性电极仅为氧化或还原反应提供表面,而不参与反应本身。它充当催化剂和导电体。
常见的惰性电极包括铂 (Pt) 和石墨 (碳)。当被氧化或还原的物质是溶液中的离子或气体时,会使用它们。
特殊情况:双极电极
双极电极是一种放置在电解质溶液中但不直接连接到电源的特殊导体。
它同时作为面向主阴极一侧的阳极和面向主阳极一侧的阴极发挥作用,从而在一个电池内实现一系列反应。
做出正确决策
您对电极的理解应指导您如何分析电化学系统。“电极类型”由其在电池中的上下文定义。
- 如果您正在分析电池(原电池): 将氧化发生的位置识别为负极阳极,将还原发生的位置识别为正极阴极。
- 如果您正在分析电解过程(例如电镀): 将连接到正极的电极识别为阳极(氧化),将连接到负极的电极识别为阴极(还原)。
- 在设计实验时: 您必须决定是需要参与反应的活性电极,还是仅用于促进溶液中已存在物质之间反应的惰性电极。
通过关注功能和材料参与,您可以准确描述和预测任何电化学系统中任何电极的行为。
总结表:
| 分类 | 类型 | 关键作用 | 常见示例 |
|---|---|---|---|
| 按功能 | 阳极 | 氧化反应的场所(失去电子) | 因电池类型而异 |
| 阴极 | 还原反应的场所(获得电子) | 因电池类型而异 | |
| 按材料 | 活性 | 参与反应 | 锌、铜 |
| 惰性 | 提供反应表面(非反应性) | 铂、石墨 | |
| 特殊 | 双极 | 同时作为阳极和阴极 | 用于特定电池设计 |
需要适合您电化学应用的电极吗? KINTEK 专注于高质量的实验室设备和耗材,包括由铂和石墨制成的耐用惰性电极,专为您的实验室提供精度和可靠性。让我们的专家帮助您选择最适合您研究或过程的组件。立即联系我们 讨论您的具体需求!
图解指南
相关产品
- 实验室用甘汞银氯化汞硫酸盐参比电极
- 金属圆盘电极 电化学电极
- RRDE 旋转圆盘(圆环圆盘)电极 / 兼容 PINE、日本 ALS、瑞士 Metrohm 玻碳铂
- 旋转铂圆盘电极,用于电化学应用
- 电池实验室应用铂片电极



















