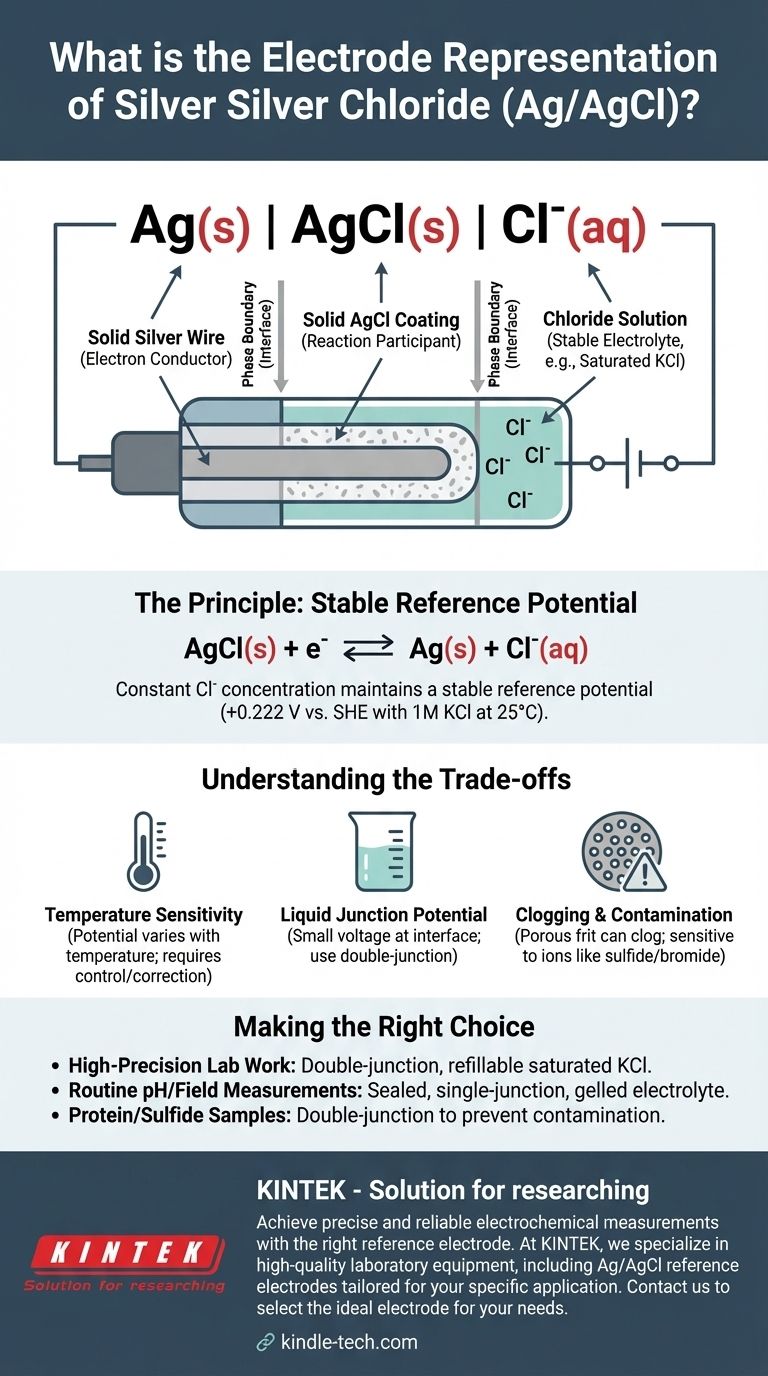
银-氯化银电极的标准缩写表示法是Ag(s) | AgCl(s) | Cl⁻(aq)。这种电化学符号描述了电极的物理和化学相,从固态银金属线到含有氯离子的水溶液。电极的具体电位关键取决于这些氯离子的浓度。
这种表示法不仅仅是一个技术标签;它是一个电化学中最可靠、最常见的参比电极之一的示意图。它描述了一个旨在维持恒定、稳定电位的系统,为准确测量其他电极的电位提供了一个固定的基准。
电极表示法的拆解
表示法Ag(s) | AgCl(s) | Cl⁻(aq)详细描述了电极的内部结构。每个组件和符号都有精确的含义。
固相:Ag(s)
这代表一根固态银线。这根线作为电子导体,将电极连接到外部测量电路(电压表或恒电位仪)。
相界:|
单竖线|表示相界。它指示了两种不同物理状态相遇的界面,在这种情况下,是固态银金属和固态氯化银层。
不溶盐层:AgCl(s)
这表示一层固态的、微溶的氯化银,直接涂覆在银线表面。这一层是电极功能的核心,直接参与电化学反应。
第二相界:|
第二条竖线标志着固态氯化银涂层与周围水性电解质溶液之间的界限。
电解质溶液:Cl⁻(aq)
这表示浸泡涂层线的水溶液。该溶液必须含有已知且恒定浓度的氯离子(Cl⁻)。通常使用氯化钾(KCl)溶液,通常是特定浓度,如1 M,或最常见的饱和溶液。

参比电极的原理
Ag/AgCl电极因其稳定性而受到重视,而不是其自身的反应。它提供了一个恒定的电压,作为其他测量的可靠零点。
控制反应
稳定的电位是通过固态组分与溶液中氯离子之间的可逆平衡建立的。半反应为:
AgCl(s) + e⁻ ⇌ Ag(s) + Cl⁻(aq)
只要溶液中氯离子的浓度(更准确地说是活度)保持恒定,该半电池的电位就不会改变。
恒定氯离子浓度的重要性
使用饱和KCl溶液可确保Cl⁻浓度恒定且可重现。如果一些水蒸发,更多的KCl盐会溶解以维持饱和。这就是参比电位如此稳定的原因。对于25°C(298 K)下的1M KCl溶液,该电位相对于标准氢电极(SHE)为+0.222 V。
了解权衡
虽然Ag/AgCl电极非常可靠,但它并非没有局限性,在进行精确工作时需要考虑。
温度敏感性
电极的电位是温度的函数。对于高精度测量,必须控制电池的温度,或者必须对测量电位进行温度变化校正。
液接电位
当电极的KCl溶液与不同的样品溶液接触时,在界面处会产生一个称为液接电位的小电压。这会给测量带来一个微小但系统性的误差,可以使用双液接电极将其最小化。
堵塞和污染
允许内部溶液与样品之间进行电接触的多孔烧结体可能会堵塞。它也可能被样品中的离子(如硫化物、溴化物或碘化物)污染,这些离子会与银反应,导致电极电位随时间漂移。
为您的测量做出正确选择
您的应用决定了哪种电极配置是最佳的。
- 如果您的主要关注点是高精度实验室工作:使用双液接Ag/AgCl电极,配备可填充的饱和KCl溶液,以最大程度地减少液接电位并便于维护。
- 如果您的主要关注点是常规pH或现场测量:密封的单液接电极,带有凝胶电解质,耐用、维护成本低且完全适用。
- 如果您的主要关注点是分析含有蛋白质或硫化物的样品:您必须使用双液接电极,以防止主要参比液接堵塞和污染。
理解这种表示法将其从一个神秘的标签转变为可靠电化学测量的功能示意图。
总结表:
| 组件 | 符号 | 描述 |
|---|---|---|
| 固态银线 | Ag(s) | 连接到外部电路的导体。 |
| 氯化银涂层 | AgCl(s) | 使可逆反应成为可能的不溶盐层。 |
| 氯离子溶液 | Cl⁻(aq) | 具有恒定Cl⁻浓度的水性电解质(例如KCl)。 |
| 相界 | | |
使用正确的参比电极,实现精确可靠的电化学测量。
在KINTEK,我们专注于高质量的实验室设备,包括一系列Ag/AgCl参比电极,可根据您的特定应用量身定制——无论您需要用于敏感实验室工作的高精度双液接型号,还是用于常规分析的耐用、低维护选项。
我们的专家可以帮助您选择理想的电极,以确保电位稳定,最大限度地减少误差,并提高您的研究准确性。
立即联系KINTEK,讨论您的实验室需求,并了解我们可靠的耗材和设备如何支持您的工作。
图解指南