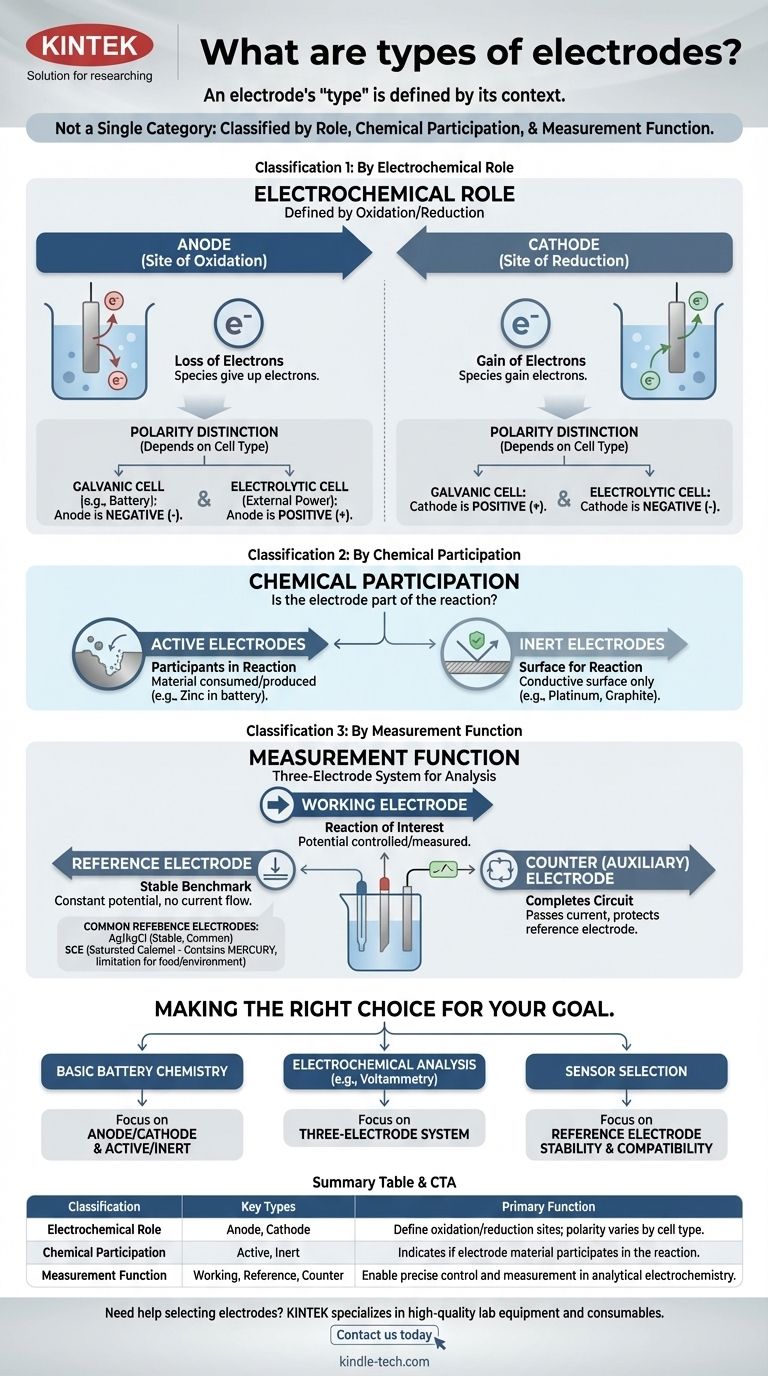
“电极”一词并非单一类别。相反,电极根据其在反应中的作用、化学参与程度以及在测量系统中的功能,分为几种不同的类型。理解这些不同的分类系统是掌握它们在任何电化学电池中目的的关键。
最关键的见解是,电极的“类型”由其所处的环境决定。同一块金属可以是阳极或阴极,活性或惰性,这完全取决于你将其置于何种电化学系统中。
分类1:按电化学作用
最基本的分类是根据电极在电化学反应的两个半反应中的作用来定义:氧化和还原。
阳极:氧化发生的地方
阳极,根据定义,是发生氧化(失去电子)的电极。阳极处的物质将其电子释放给电极。
阴极:还原发生的地方
阴极是发生还原(获得电子)的电极。阴极将其电子提供给溶液中的物质。
关键区别:阳极/阴极的极性
一个常见的混淆点是阳极和阴极的电荷(+或-)。这种极性取决于电池的类型:
- 在原电池(如电池)中,自发反应产生能量。阳极是负极,阴极是正极。
- 在电解池中,外部电源驱动非自发反应。阳极是正极,阴极是负极。
分类2:按化学参与程度
此分类描述电极材料本身是否参与化学反应。
活性电极:反应的参与者
活性电极由在电池反应过程中被消耗或生成的材料制成。例如,在锌铜电池中,锌阳极溶解,积极参与氧化半反应。
惰性电极:反应的表面
惰性电极不参与化学反应。它仅作为导电表面,供氧化或还原发生。铂和碳(石墨)是常用的惰性电极,用于促进涉及气体或溶解离子的反应。
分类3:按测量功能
在分析电化学中,常使用三电极系统进行精确测量。这产生了功能性分类。
工作电极
这是发生目标反应的电极。其电位是主要被控制或测量的变量。
参比电极:稳定的基准
参比电极提供一个稳定、恒定的电位,工作电极的电位就是以此为基准进行测量。无论电流如何流动或主体溶液的组成如何,其自身的电位都不会改变。
对电极(或辅助电极)
此电极的唯一目的是完成电路。它通过工作电极所需的所有电流,确保流经敏感参比电极的电流可忽略不计,从而保护其稳定性。
理解权衡:常用参比电极
参比电极的选择对于精确测量至关重要,并取决于化学环境。
Ag/AgCl:常用的主力军
银/氯化银(Ag/AgCl)电极是最常见的参比电极。它稳定、价格低廉且通常可靠,是许多水溶液的默认选择。
饱和甘汞电极(SCE):经典的替代品
饱和甘汞电极(SCE)是一种较旧、高度稳定的标准。它常用于样品溶液与银或氯离子不兼容的情况,因为这些离子可能会干扰Ag/AgCl电极。
汞问题:一个主要限制
SCE的主要缺点是它含有汞。这使得它不适用于涉及食品、饮料或环境测试的应用,因为汞污染是一个重大问题。
根据您的目标做出正确选择
您的应用决定了哪种分类最重要。
- 如果您的主要重点是理解基本的电池化学:掌握阳极/阴极和活性/惰性电极的概念。
- 如果您的主要重点是进行电化学分析(如伏安法):三电极系统(工作、参比、对电极)是基本框架。
- 如果您的主要重点是为特定环境选择传感器:您主要关注的是参比电极的化学兼容性和稳定性,例如在Ag/AgCl和其他替代品之间进行选择。
理解这些重叠的分类使您能够控制和解释任何电化学系统的行为。

总结表:
| 分类 | 主要类型 | 主要功能 |
|---|---|---|
| 电化学作用 | 阳极,阴极 | 定义氧化/还原位点;极性因电池类型(原电池/电解池)而异 |
| 化学参与程度 | 活性,惰性 | 指示电极材料是否参与反应或仅作为表面 |
| 测量功能 | 工作,参比,对电极 | 在分析电化学中实现精确控制和测量 |
需要帮助为您的实验室电化学应用选择合适的电极吗?在KINTEK,我们专注于提供高质量的实验室设备和耗材,以满足您的研究需求。无论您是从事电池开发、传感器设计还是分析测量,我们的专业知识都能确保您获得最佳的电极,以实现准确性和性能。立即联系我们,讨论您的需求并提升您的电化学工作流程!
图解指南
相关产品
- 实验室用甘汞银氯化汞硫酸盐参比电极
- 金属圆盘电极 电化学电极
- RRDE 旋转圆盘(圆环圆盘)电极 / 兼容 PINE、日本 ALS、瑞士 Metrohm 玻碳铂
- 旋转铂圆盘电极,用于电化学应用
- 电池实验室应用铂片电极



















