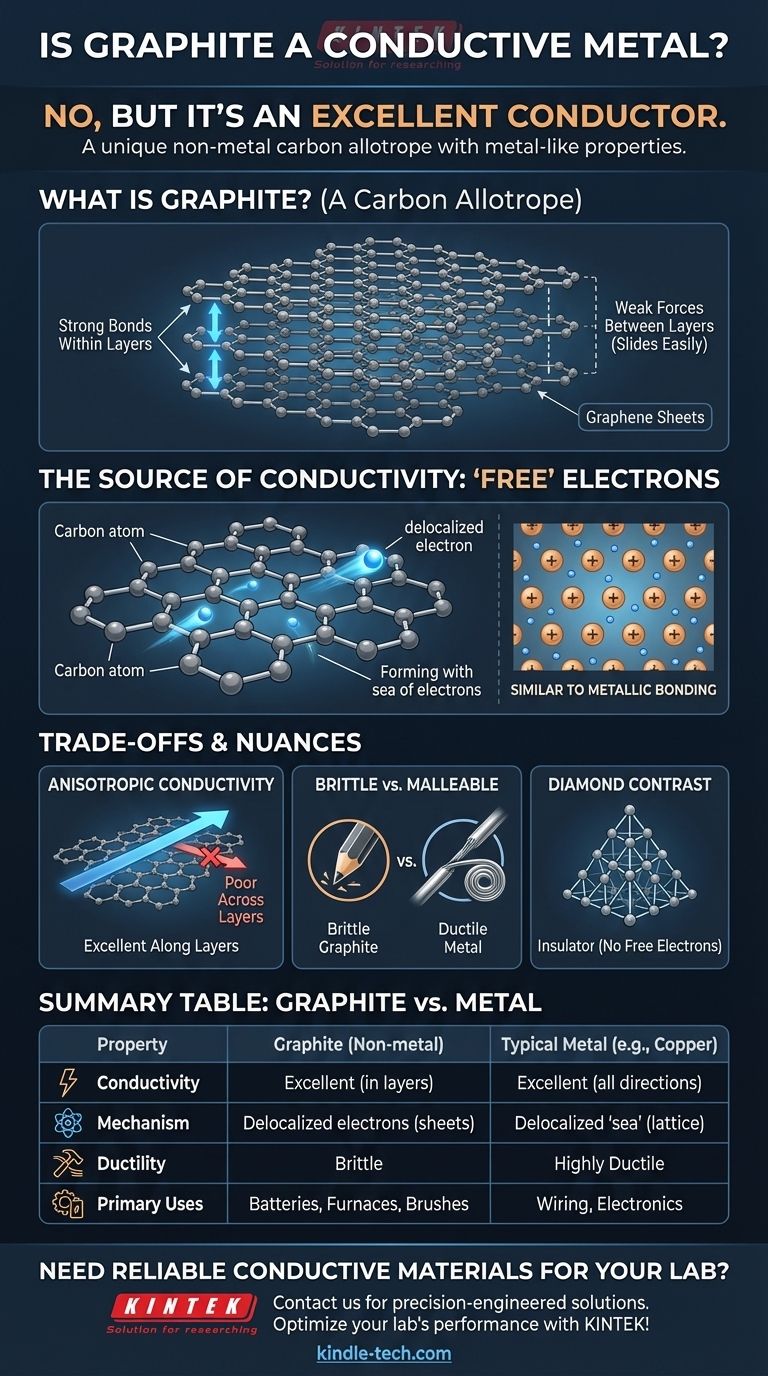
不,石墨不是金属,但它是一种优良的电导体。这种区别经常引起混淆,因为我们通常被教导将导电性 exclusively 与金属元素联系起来。石墨是碳这种非金属元素的同素异形体——一种特定的结构形式。
这种混淆的核心原因是我们倾向于根据简单的类别而不是其基本结构来对材料进行分组。石墨虽然是一种非金属,但它能导电,因为其独特的层状原子排列产生了“自由”电子,这些电子的行为几乎与真正金属中的电子完全相同。
什么是石墨?一种独特的碳形式
石墨的性质直接源于其独特的原子结构。理解这种结构是理解其行为的关键。
不是金属,而是同素异形体
元素可以以不同的物理形式存在,称为同素异形体。这些形式具有相同的原子,但结构排列不同,这赋予它们截然不同的性质。
石墨是碳的一种同素异形体。最著名的另一种碳同素异形体是金刚石。尽管两者都是纯碳,但它们的结构使石墨成为柔软的导体,而金刚石则成为坚硬的绝缘体。
堆叠层结构
石墨由无数堆叠在一起的扁平薄片组成。每个薄片,称为石墨烯,是碳原子以蜂窝状六边形晶格排列的单原子厚层。
薄片内将原子结合在一起的键非常强。然而,将不同薄片相互结合在一起的力非常弱,使它们能够轻易滑动。这就是为什么石墨柔软易碎,形成铅笔中的“铅”。

石墨导电性的来源
石墨导电的原因在于其电子的共享方式——或者更确切地说,是不共享方式。这模仿了金属的导电机制,而石墨本身并非金属。
碳电子的作用
每个碳原子有四个可用于键合的外层电子(价电子)。在石墨烯薄片的六边形结构中,每个碳原子与三个相邻原子形成强共价键。
“自由”离域电子
这使得四个价电子中的一个未被占据。这个第四个电子不被锁定在两个特定原子之间的键中。相反,它变得离域,可以在其二维石墨烯薄片上自由移动。
非金属中的“电子海”
这些离域电子的集合在每个层内形成了一个移动的“电子海”。由于电流仅仅是电子的流动,这些自由移动的电子使石墨能够轻松导电。
这与金属键合基本相似,金属键合中,正金属离子晶格位于共享的、离域电子的“海洋”中。石墨通过完全不同的原子结构实现了类似的结果。
理解权衡和细微之处
虽然石墨是一种导体,但它不能完美替代金属。其非金属性质伴随着明显的权衡。
导电性不均匀
石墨具有高度的各向异性,这意味着其性质取决于方向。它在石墨烯薄片内导电性极佳,但在薄片之间导电性极差。相比之下,大多数金属是各向同性的,在所有方向上导电性都一样好。
脆性与延展性
金属通常具有延展性和可塑性,这意味着它们可以被拉成线或锤打成新形状而不断裂。石墨是脆性的,在类似的应力下会破碎。你不能通过拉伸来形成石墨线。
金刚石:绝缘的对应物
金刚石提供了完美的对比。在其刚性的四面体晶格中,每个碳原子与四个其他原子键合,用尽了所有四个价电子。由于没有离域电子,没有自由移动并携带电流的物质,这使得金刚石成为一种优良的电绝缘体。
为您的应用做出正确选择
理解这些原理使您能够根据任务所需的特定性质选择正确的材料。
- 如果您的主要关注点是柔性、全向导电性:铜和铝等金属由于其延展性和各向同性性质仍然是优越的选择。
- 如果您的主要关注点是用于高温的轻质、化学稳定导体:石墨是电池电极、炉衬和电机电刷等应用的理想材料。
- 如果您的主要关注点是硬度和电绝缘性:金刚石,碳的另一个著名同素异形体,是解决方案,证明原子排列决定一切。
最终,材料的性质由其原子结构决定,而不是由我们对其进行简单分类。
总结表:
| 性质 | 石墨 | 典型金属(例如铜) |
|---|---|---|
| 材料类型 | 非金属(碳同素异形体) | 金属 |
| 导电性 | 极佳(层内) | 极佳(所有方向) |
| 导电机制 | 石墨烯薄片中的离域电子 | 离域的“电子海” |
| 延展性/可塑性 | 脆性,不能拉成线 | 高度延展和可塑 |
| 主要用途 | 电池、炉衬、电机电刷 | 电线、结构部件、电子产品 |
您的实验室应用需要可靠的导电材料吗?无论您是在处理高温炉、电池研究还是定制电极设置,KINTEK 在实验室设备和耗材方面的专业知识都能确保您获得正确的解决方案。我们的团队可以帮助您选择符合您特定导电性、温度和耐用性要求的材料。立即联系我们,通过 KINTEK 精密工程解决方案优化您的实验室性能!
图解指南