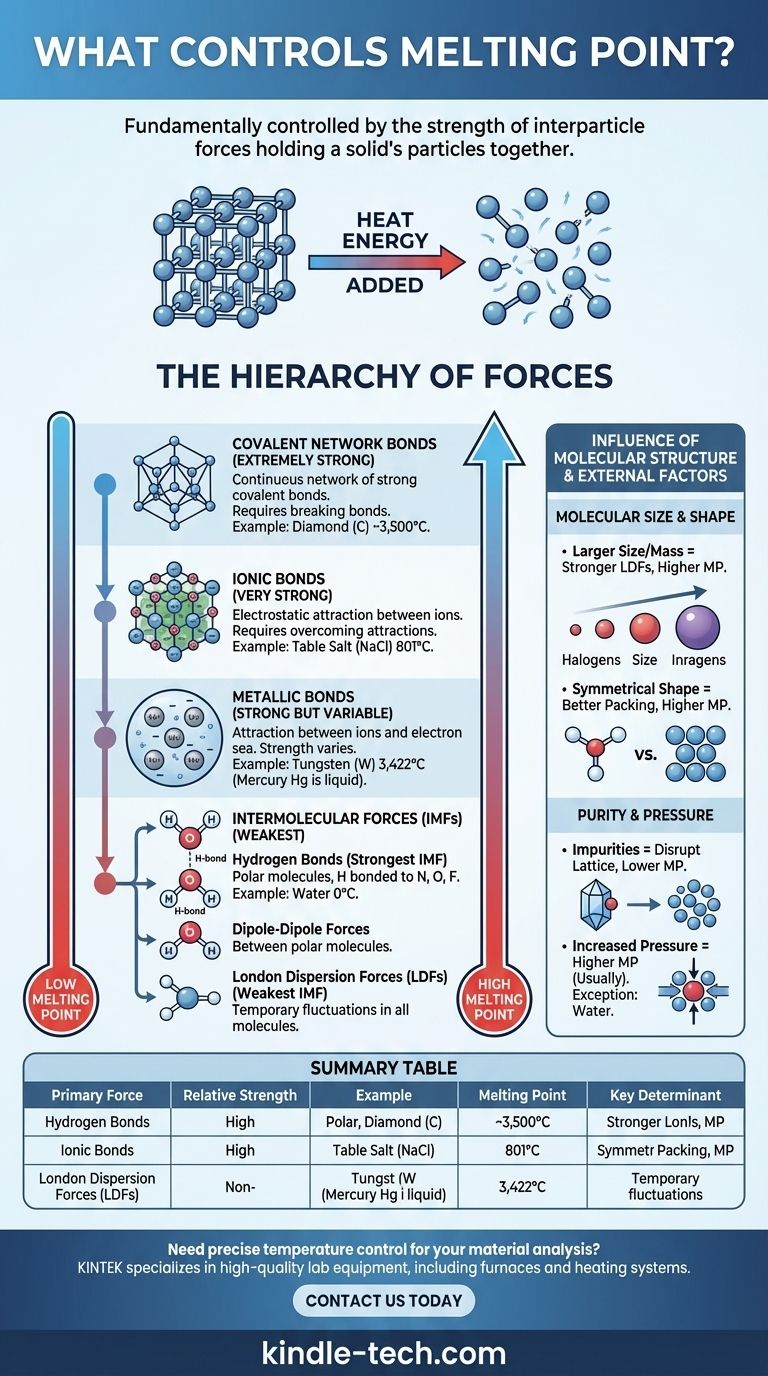
物质的熔点从根本上取决于将其粒子束缚在一起的作用力强度。在固体中,粒子(原子、离子或分子)被锁定在称为晶格的固定有序排列中。要熔化固体,必须加入足够的热能,使这些粒子能够克服这些作用力,并像液体一样相互移动。因此,作用力越强,打破所需的能量就越多,熔点也就越高。
核心原则很简单:熔化不是要打破粒子本身,而是要克服它们之间的吸引力。这些粒子间作用力的类型和强度——从强大的离子键到弱的分子间吸引力——是物质熔点的首要决定因素。
作用力层级
熔点的巨大差异——从氢的-259°C到钨的3,422°C——可以通过对束缚固体的作用力进行分类来理解。这些作用力存在一个清晰的强度层级。
离子键(非常强)
在食盐 (NaCl) 等离子化合物中,粒子是带正电荷和负电荷的离子。它们通过强大的静电吸引力被束缚在一个坚硬的晶格中。
克服这些强大的离子键需要巨大的热能。因此,离子化合物通常表现出非常高的熔点。
共价网络键(极强)
在共价网络固体中,原子通过一个巨大的、连续的强共价键网络连接在一起。没有单个分子;整个晶体本质上是一个巨大的分子。
金刚石(碳)和石英(二氧化硅)是典型的例子。要熔化它们,必须打破这些极强的共价键,这需要巨大的能量,从而导致极高的熔点。
金属键(强但可变)
金属由正金属离子晶格组成,这些离子位于一个“电子海”中,电子在整个结构中自由移动。正离子与这个电子海之间的吸引力构成了金属键。
该键的强度,以及熔点,差异很大。它取决于离子电荷和离域电子数等因素。这就是为什么汞在室温下是液体,而钨是所有元素中熔点最高的元素之一。
分子间作用力(最弱)
对于分子化合物(如水、糖或蜡),熔化时必须克服的作用力是分子间作用力 (IMFs)——即单个分子之间的吸引力。这些比上述离子键、共价键或金属键要弱得多。
IMFs有三种主要类型:
- 氢键:最强的IMF类型。它发生在极性分子中,其中氢直接与高电负性原子(氮、氧或氟)键合。水相对较高的熔点(0°C)归因于这些强大的氢键。
- 偶极-偶极力:发生在具有永久正负端的极性分子之间。这些作用力比氢键弱。
- 伦敦色散力 (LDFs):最弱的IMF,存在于所有分子中。它们源于电子分布中临时、随机的波动。尽管单个作用力很弱,但它们累积起来对大分子可能产生显著影响。

分子结构的影响
除了作用力的类型,粒子的大小和形状也起着关键作用,特别是对于分子化合物。
分子大小和质量
对于具有相同主要分子间作用力(例如 LDFs)的化合物,分子越大,熔点越高。这是因为较大的分子具有更多的电子,产生了更具“极化性”的电子云,从而导致更强的伦敦色散力。
这种趋势在卤素中很明显:从氟 (F₂) 到碘 (I₂),熔点增加。
分子形状和堆积效率
分子紧密有效地堆积到晶格中的能力有很大影响。对称分子通常比不对称异构体具有更高的熔点,即使它们的分子式和质量相同。
对称的形状使分子能够在固态中更紧密地结合在一起,最大限度地发挥其分子间作用力的效果。打破这种组织良好的结构需要更多的能量。
理解权衡和细微差别
预测熔点需要权衡这些相互关联的因素。
纯度决定一切
上述原理假设物质是纯净的。杂质会破坏有序的晶格,削弱整体结构。
这种破坏使得固体更容易熔化。因此,杂质的熔化温度会更低,并且熔化范围比其纯净对应物更宽。这种现象被称为熔点降低。
压力起作用
熔点通常是在标准大气压下测定的。对于大多数物质,增加压力会提高熔点,因为它会物理地将粒子推得更近,从而增强晶格结构。
水是一个著名且关键的例外。因为固态冰的密度低于液态水,增加的压力有利于更密集的液相,从而降低熔点。
如何在分析中应用
在比较物质时,请使用系统化的方法来确定起作用的关键因素。
- 如果您的主要重点是比较不同类别的固体:首先,确定主要的结合力——离子键、共价网络键、金属键或分子间作用力。这将为您提供熔点相对程度的最重要指标。
- 如果您的主要重点是比较两种分子化合物:确定它们各自拥有的最强的分子间作用力(氢键 > 偶极-偶极力 > LDFs)。具有更强 IMF 的化合物通常熔点更高。
- 如果您的主要重点是相似的非极性分子:质量和表面积更大的分子将具有更强的伦敦色散力,因此熔点更高。
- 如果您的主要重点是异构体(相同分子式,不同形状):能够更有效地堆积到晶格中的更对称的分子通常具有更高的熔点。
通过理解这种作用力层级和结构的影响,您可以系统地解释几乎任何物质的熔化行为。
总结表:
| 主要作用力类型 | 相对强度 | 示例物质 | 熔点 | 关键决定因素 |
|---|---|---|---|---|
| 共价网络 | 极强 | 金刚石 (C) | ~3,500°C | 打破连续晶格中的共价键 |
| 离子键 | 非常强 | 氯化钠 (NaCl) | 801°C | 克服离子之间的静电吸引力 |
| 金属键 | 强(可变) | 钨 (W) | 3,422°C | 离子-电子海吸引力的强度 |
| 分子间作用力 | 最弱 | 水 (H₂O) | 0°C | 氢键、偶极-偶极力、伦敦色散力 |
需要对材料分析进行精确的温度控制吗?了解熔点对于可靠的实验结果至关重要。在 KINTEK,我们专注于高质量的实验室设备,包括专为精确热分析而设计的熔炉和加热系统。无论您是处理高熔点金属还是敏感的分子化合物,我们的解决方案都能确保一致的性能。立即联系我们,讨论我们的产品如何增强您实验室的能力并支持您的研究。请通过我们的联系表单联系我们以开始!
图解指南