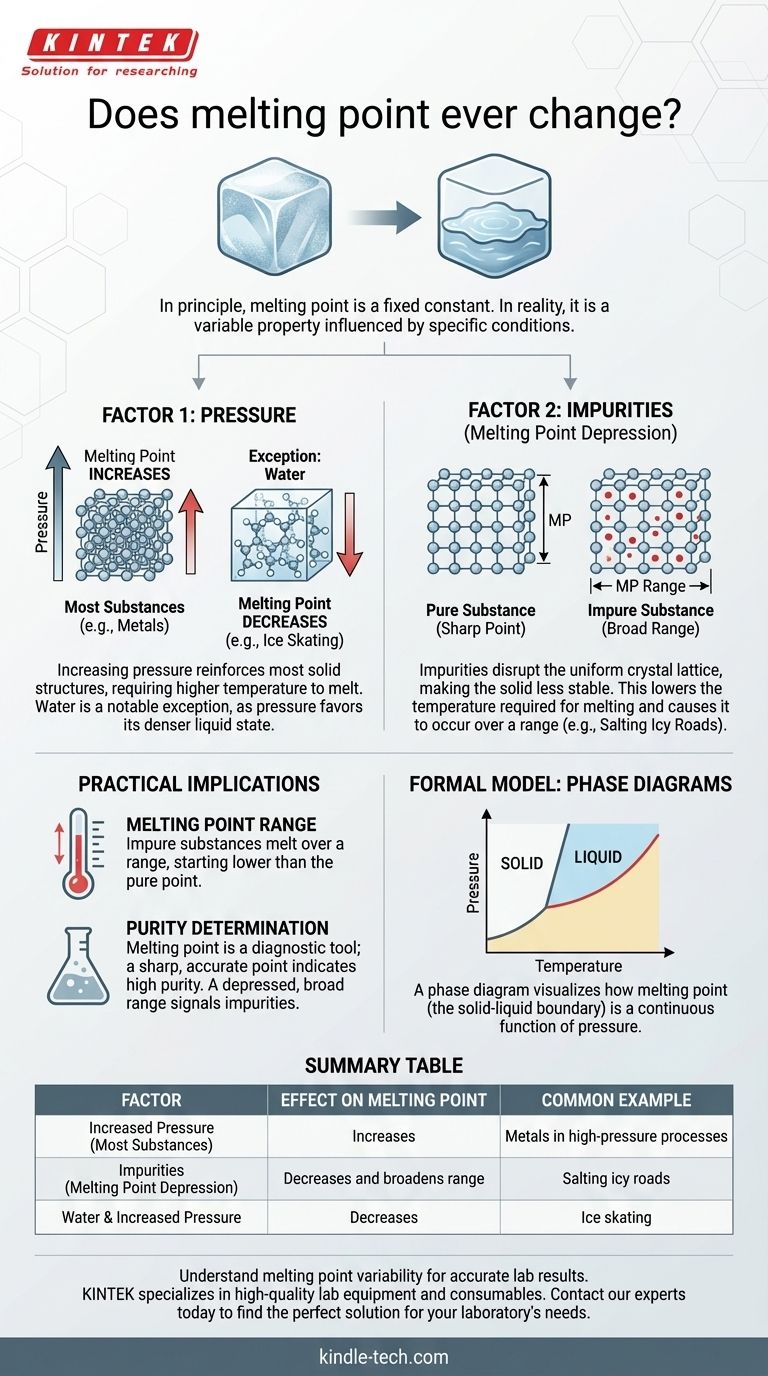
原则上,纯物质的熔点是一个固定的物理常数。然而,在现实世界中,观察到的物质熔化温度绝对会改变。这并非任意的转变;它是对两个主要因素的可预测响应:环境压力的变化和杂质的引入。
虽然教科书通常将熔点呈现为一个静态数字,但更准确的理解是,它是一种属性,并且仅在特定条件下保持不变。了解压力和纯度如何影响这一属性是预测和控制其在任何实际应用中行为的关键。
改变熔点的两个因素
物质的“官方”熔点,例如水在0°C(32°F)时的熔点,是在标准条件下测量的——通常是在一个大气压下,且物质处于高度纯净的状态。当这些条件不满足时,熔点就会发生偏差。
因素1:压力的影响
对于大多数物质,增加外部压力会迫使分子排列得更紧密。这会增强固体结构,需要更多的能量(更高的温度)才能打破键并转变为液体。
因此,对于绝大多数材料,压力的增加会导致熔点的升高。
然而,有一个关键且著名的例外:水。固态水(冰)比液态水密度小,这就是冰山浮在水面上的原因。对冰施加压力有利于密度更大的状态——液态水。这意味着在更高的压力下,冰会在更低的温度下融化。这就是为什么溜冰刀片通过在细线上施加高压,可以产生一层微观的水膜以供滑行。
因素2:杂质的作用
这是在高压实验室之外,熔点发生变化最常见的原因。当你将杂质(溶质)引入纯物质(溶剂)中时,它会破坏固体的均匀、重复的晶格。
这种破坏使得固体结构变得不稳定。因此,打破它并将其转化为液体所需的能量更少。这种现象被称为熔点降低。
一个经典的例子是给结冰的道路撒盐。盐与冰混合,降低了冰的熔点。这使得冰即使在环境气温仍低于水的正常冰点时也能融化。

理解实际意义
认识到熔点可以改变不仅仅是学术上的探讨。它在科学和工业环境中具有重要意义,在这些环境中,它经常被用作诊断工具。
从“点”到“范围”
纯结晶固体通常在非常尖锐、特定的温度下熔化。当你开始加热它时,温度会升高,直到达到熔点,在那里温度保持稳定,直到所有固体都变成液体。
不纯物质的行为则不同。它不会在单一温度下熔化,而是在一个熔点范围内熔化。熔化开始的温度低于纯物质,并在接近(但通常仍低于)纯物质熔点的温度下完成。
利用熔点确定纯度
这个“缺陷”实际上是一个非常有用的特性。在化学实验室中,评估合成结晶化合物纯度的首批最快方法之一就是测量其熔点。
如果化合物在较宽的范围内熔化,并且熔化温度低于文献值,则清楚地表明存在杂质,需要进一步纯化。与既定值匹配的尖锐熔点是高纯度的有力指标。
正式模型:相图
压力、温度和物质状态(固态、液态、气态)之间的关系在相图中正式体现。
物理状态图
相图是一个以压力为y轴,温度为x轴的图表。图表上的线条划定了物质在不同相之间转变的边界。
固液边界
该图上将固相与液相分开的线代表了在所有可能压力下的熔点。查看此图可以立即清楚地看出,熔点不是一个单一的数字,而是压力的连续函数。这个视觉模型统一了概念,并证明了熔点本质上是可变的。
为您的目标做出正确选择
您对熔点的看法应由您的目标决定。
- 如果您的主要重点是化学合成或分析:将熔点视为纯度的关键诊断工具。尖锐、准确的熔点证实了成功,而降低、宽泛的范围则表明需要纯化。
- 如果您的主要重点是材料科学或工程:您必须在设计中考虑压力变化。材料在海平面上的熔点可能与高压工业过程或深地应用中的熔点不同。
- 如果您的主要重点是理解日常现象:利用熔点降低原理来解释为什么我们在冬天给道路撒盐,或者为什么在冰水浴中加盐会使其变得更冷,以便制作冰淇淋。
最终,认识到熔点是一个动态属性,而不是一个静态数字,将其从一个简单的事实转变为一个强大的预测工具。
总结表:
| 因素 | 对熔点的影响 | 常见例子 |
|---|---|---|
| 压力增加 | 升高(对于大多数物质) | 高压工艺中的金属 |
| 杂质(熔点降低) | 降低并扩大范围 | 给结冰的道路撒盐 |
| 水与压力增加 | 降低 | 溜冰 |
您的实验室工作需要精确的温度控制吗?
了解熔点变异性对于准确的合成和分析至关重要。KINTEK 专注于高质量的实验室设备和耗材,包括熔点仪,旨在提供您的实验室所需的可靠性和精确度。
让我们帮助您获得一致、准确的结果。 立即联系我们的专家,为您的实验室需求找到完美的解决方案。
图解指南