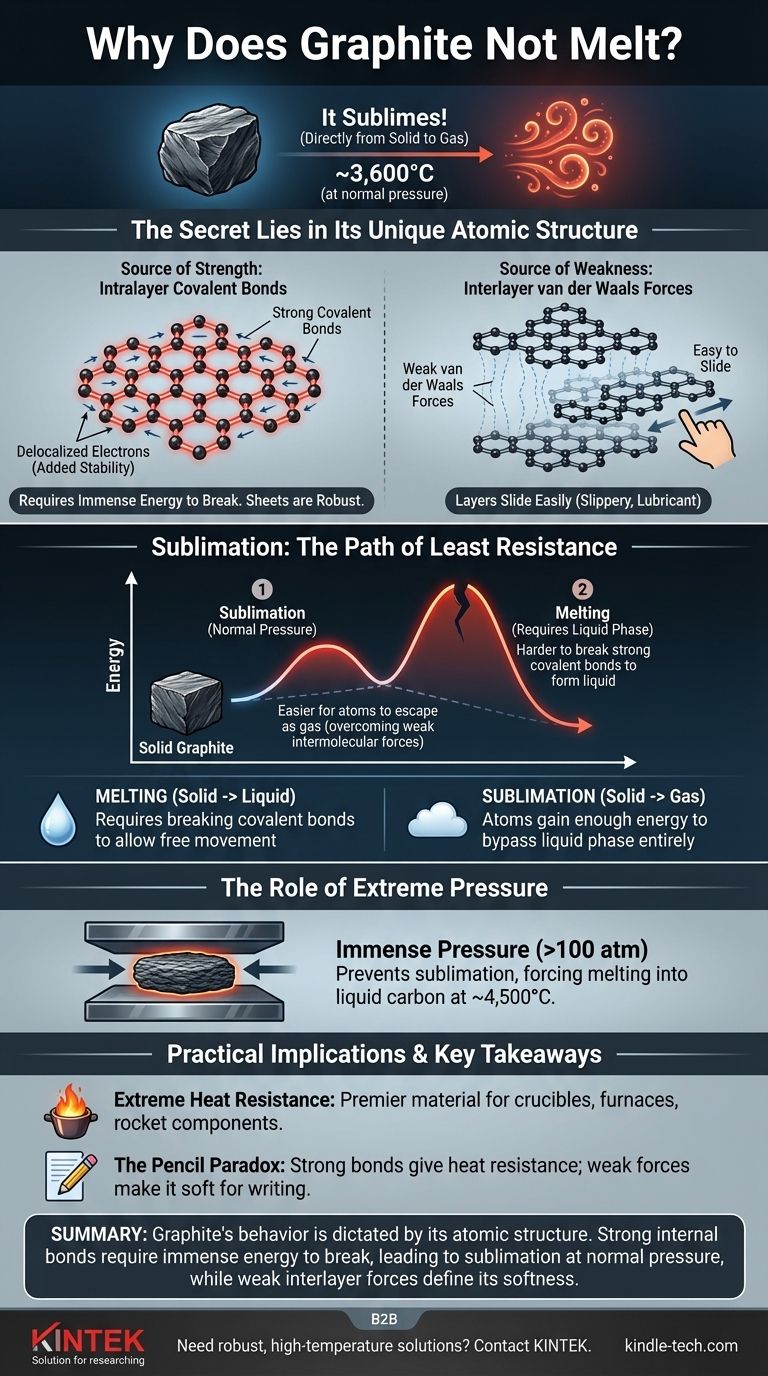
石墨不熔化是一个常见的误解。 在正常大气压下,石墨会发生不同的现象:它会升华,在约3,600°C (6,500°F) 的极高温度下直接从固体变为气体。这种行为直接源于其碳原子之间巨大的化学键强度。
石墨具有极致耐热性的核心原因是其独特的原子结构。它由碳原子层组成,这些碳原子层通过异常强大的共价键连接,需要巨大的能量才能断裂并使物质改变状态。
解构石墨的原子结构
要理解石墨为何表现出这种行为,我们必须审视其碳原子的排列方式。其结构由两种截然不同的化学键同时作用所决定。
强度的来源:层内的共价键
石墨由扁平的二维碳原子片组成,这些碳原子呈六边形蜂窝状晶格排列。
在每个片层内,每个碳原子都通过强共价键与另外三个碳原子连接。这些是自然界中最强大的化学键之一。
此外,每个碳原子中的一个电子会离域,这意味着它可以在整个片层中自由移动。这种电子在所有原子间的共享显著增加了稳定性,并进一步加强了键,使得这些片层异常坚固且难以分离。
弱点的来源:层间的力
虽然层内的原子通过强大的键连接,但层与层之间则通过弱得多的力(称为范德华力)结合在一起。
这些力足够弱,使得层可以轻易地相互滑动。这就是为什么石墨摸起来滑腻,并被用作润滑剂和铅笔芯——书写时会在纸上留下石墨层。

升华:阻力最小的路径
层内强键与层间弱力之间的巨大差异决定了石墨对热的反应方式。
熔化与升华
熔化是固体变为液体的过程。要发生这种情况,原子必须获得足够的能量以摆脱其固定位置,但仍保持相互吸引。
升华是固体直接转变为气体的过程。在这种情况下,原子获得如此多的能量,以至于它们完全跳过液相并逸散到空气中。
为何在常压下升华占优
在标准大气压下,打破石墨层内强大共价键所需的能量是巨大的。
在结构吸收足够能量熔化成液体之前,表面原子会获得足够的能量来克服弱分子间力,并简单地以气体形式逸出。对于原子来说,直接进入气态比打破形成液体所需的共价键在能量上更容易。
极端压力的作用
石墨可以被强制熔化,但仅限于特殊条件。
通过施加巨大的压力(超过正常大气压的100倍),可以阻止碳原子以气体形式逸出。在这些条件下,石墨将在约4,500°C (8,132°F) 的温度下熔化成液态碳。
这种结构的实际应用
这种独特的双键结构赋予了石墨一系列看似矛盾但对其工业应用至关重要的特性。
极致耐热性
高升华点使石墨成为高温环境下的首选材料。它被用于制造熔化金属的坩埚、炉衬以及必须承受巨大热量的火箭发动机部件。
铅笔悖论
石墨的结构解释了它为何既能极度耐热又出奇地柔软。强度来自层内的共价键,而柔软性和润滑性则来自这些层之间易于滑动的特性。
理解石墨的关键要点
- 如果您的主要关注点是其在热作用下的行为:请记住,在常压下,石墨直接升华为气体,因为这样所需的能量小于打破共价键并形成液体所需的能量。
- 如果您的主要关注点是其物理特性:关键在于其层状结构。层内的强键提供了耐热性,而层间的弱力使其柔软并成为有效的润滑剂。
- 如果您的主要关注点是熔化的技术定义:石墨绝对可以熔化,但只有在阻止原子首先升华的极高压力下才能实现。
最终,石墨的行为完美地说明了材料的原子结构如何决定其真实世界的特性。
总结表:
| 特性 | 描述 | 关键原因 |
|---|---|---|
| 升华点 | 约3,600°C(常压下) | 层间弱范德华力允许原子在熔化前以气体形式逸出。 |
| 熔点 | 约4,500°C(极端压力下 >100 atm) | 高压阻止升华,迫使共价键断裂以实现熔化。 |
| 耐热性 | 非常适合高温应用 | 碳层内极强的共价键需要巨大的能量才能断裂。 |
需要为您的实验室提供坚固耐用的高温解决方案吗?
石墨独特的特性使其成为苛刻应用中不可或缺的材料。在 KINTEK,我们专注于提供高质量的实验室设备和耗材,包括石墨坩埚和炉部件,旨在承受极端条件。
让我们的专家帮助您选择合适的材料,以提高实验室的效率和安全性。立即联系 KINTEK,讨论您的具体高温需求!
图解指南