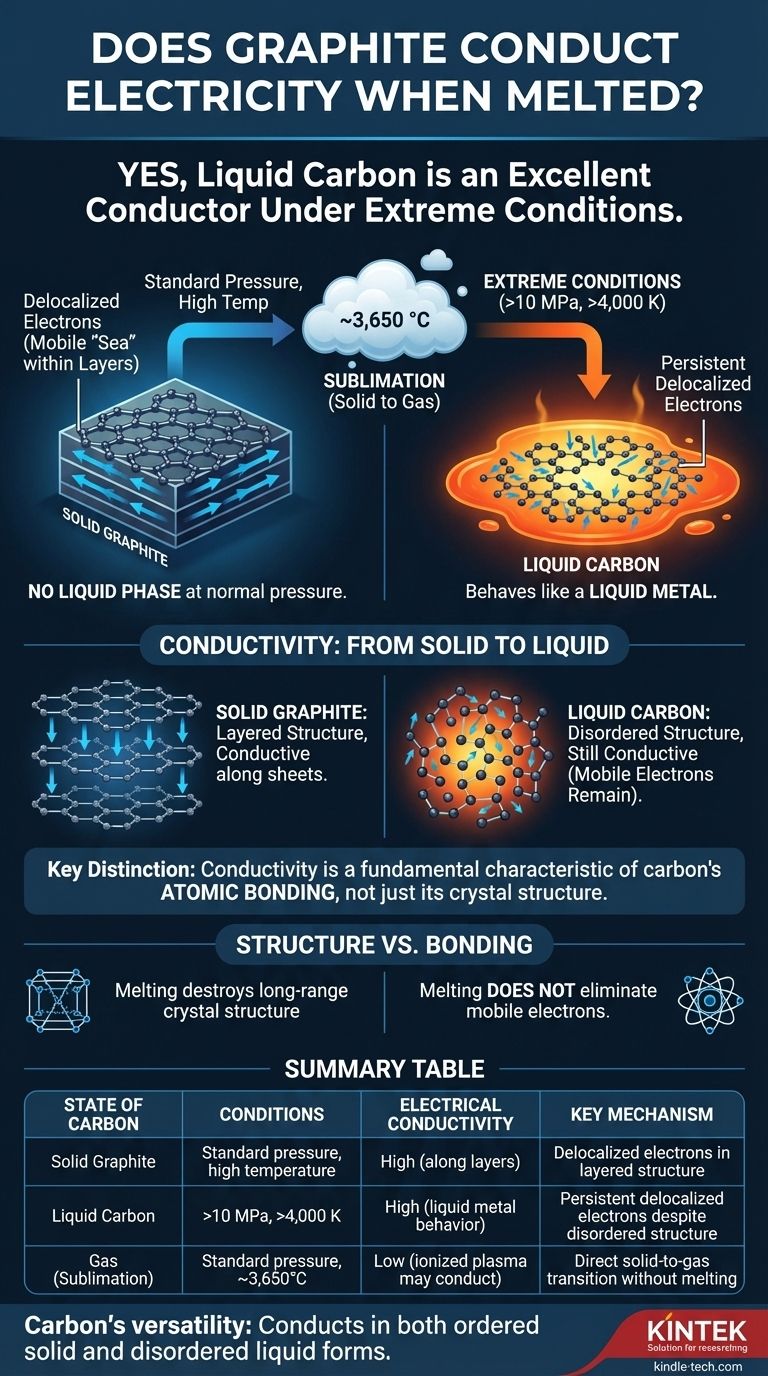
是的,在熔化所需的极端条件下,液态碳是优良的电导体。 虽然石墨在常压下不会熔化,但在极高压力和温度下形成的液态碳表现得像液态金属,电子可以自由移动并携带电流。
这个问题不仅仅是熔融石墨是否导电——它确实导电——而是为什么。答案揭示了导电性不仅仅是石墨著名的层状结构的一个特性,而是碳原子键合的一个更基本特征,即使在无序的液态中也依然存在。
熔化石墨的挑战
要理解液态碳的导电性,我们首先必须认识到制造它的难度。在大多数实际用途中,石墨没有液相。
升华,而非熔化
在标准大气压下,当你将石墨加热到极限时,它不会变成液体。相反,它会升华——在大约 3,650 °C (6,600 °F) 的温度下直接从固态转变为气态。
极端条件的需求
要迫使碳进入液态,你需要同时施加巨大的压力和温度。液态碳仅存在于高于 10 兆帕(约正常大气压的 100 倍)的压力和超过 4,000 K(约 3,727 °C 或 6,740 °F)的温度下。

导电性:从固体到液体
固体石墨和液态碳都能导电的原因在于碳电子的独特性质。
固体石墨如何导电
在固体石墨中,碳原子排列成平坦的六边形片层。每个碳原子与其三个邻居形成强键,留下其第四个外层电子离域。
这些离域电子不束缚于任何单个原子。相反,它们在每个片层内形成一个移动的电子“海洋”,这就是为什么石墨沿着其层具有优良的导电性。
液态下的导电性
当石墨被迫熔化时,其刚性的层状结构被破坏。原子变得无序并可以自由移动,就像在任何液体中一样。
然而,局部的键合环境仍然允许离域电子存在。液体是键合类型复杂且波动的混合物,但移动电子的存在仍然存在。这使得液态碳表现得像一种液态金属,具有高导电性。
理解关键区别
人们很容易认为石墨的导电性完全是其片状结构的结果。液态碳的行为证明这是一个不完整的图景。
结构与键合
关键要点是结构与键合之间的区别。虽然熔化破坏了石墨的长程晶体结构,但它并没有消除允许电子移动的基本原子键合。
实际限制
这种现象主要在极端物理学和材料科学中具有意义。在大多数工程应用中,例如在电弧炉中,你处理的是升华成热的、电离的气体(等离子体)的固体石墨电极,而不是一池液态碳。
理解碳的性质
你对这个主题的理解取决于你的目标。使用以下几点来根据你的具体背景来构建这个概念。
- 如果你的主要重点是基础化学: 液态碳的导电性证明了离域电子(碳 sp2 键合的特征)在刚性晶格结构熔化时不会丢失。
- 如果你的主要重点是实际工程: 对于几乎所有的应用,请记住石墨在有机会熔化之前就会升华成气体,这是设计高温系统的关键因素。
最终,碳在其有序固态和无序液态下都能导电的能力,揭示了其原子键合的惊人多功能性。
摘要表:
| 碳的状态 | 所需条件 | 导电性 | 关键机制 |
|---|---|---|---|
| 固体石墨 | 常压,高温 | 高(沿层) | 层状结构中的离域电子 |
| 液态碳 | >10 MPa,>4,000 K | 高(液态金属行为) | 尽管结构无序,但离域电子持续存在 |
| 气体(升华) | 常压,~3,650°C | 低(电离等离子体可能导电) | 无熔化过程的直接固-气转变 |
使用 KINTEK 在高温研究中实现精度
理解极端材料行为(如液态碳导电性)需要可靠的实验室设备。KINTEK 专注于专为严苛条件设计的高性能实验室炉、电极和易耗品。无论您是探索材料科学还是开发先进的工程系统,我们的产品都能确保准确性和耐用性。
准备好提升您的实验室能力了吗? 立即联系我们,讨论 KINTEK 的解决方案如何支持您的极端温度实验和研究目标。
图解指南